 |
 |

Gestion des soins gériatriques pour personnes âgées à revenus modestesUn essai contrôlé randomisé
Steven R. Counsell, MD;
Christopher M. Callahan, MD;
Daniel O. Clark, PhD;
Wanzhu Tu, PhD;
Amna B. Buttar, MD, MS;
Timothy E. Stump, MS;
Gretchen D. Ricketts, BSW
RÉSUMÉ
 |  |
Contexte Les personnes âgées à revenus modestes
souffrent fréquemment de multiples affections médicales
chroniques pour lesquelles elles ne reçoivent pas les traitements
recommandés.
Objectifs Tester l'efficacité d'un modèle de gestion
des traitements gériatriques visant à améliorer la
qualité des soins primaires prodigués aux personnes
âgées à revenus modestes.
Schéma, environnement et participants Un essai clinique
contrôlé chez 951 adultes âgés de 65 ans et plus
dont le revenu annuel atteint moins de 200 % du niveau fédéral
de pauvreté. Les médecins traitant ces patients dans des centres
publics de santé ont, de janvier 2002 à août 2004,
été répartis de manière aléatoire entre un
groupe d'intervention (474 patients) et un groupe des soins habituels (477
patients).
Intervention Dans le groupe d'intervention, les patients ont
reçu deux ans de soins à domicile prodigués par un
infirmier diplômé et un travailleur social qui ont
collaboré avec le médecin généraliste et une
équipe interdisciplinaire de soins gériatriques. Les
intervenants se sont référés à 12 protocoles de
traitements conçus pour les conditions gériatriques
habituelles.
Principaux critères de jugement Les échelles et
évaluations médicales spécifiées dans le SF-36
(questionnaire à 36 éléments), les activités
instrumentales et de base de la vie quotidienne (AVQ), les visites aux
services des urgences (SU) sans hospitalisation et les hospitalisations.
Résultats L'analyse à 24 mois en intention de traiter
a révélé, chez les patients du groupe d'intervention, des
améliorations significatives de quatre sur huit des
éléments de la grille SF-36 : état de santé
général (0,2 vs -2.3, P=0,045), vitalité (2,6 vs -2,6,
P=0,001), comportement social (3,0 vs -2,3, P=0,008) et santé mentale
(3,6 vs -0,3, P=0,001). On a relevé par ailleurs une
amélioration du score composite mental (2,1 vs -0,3, P<0,001). Pas
de différence intergroupes pour les AVQ et la mortalité.
Cumulé à 2 ans et par 1 000, le taux des visites aux urgences
était inférieur dans le groupe d'intervention (1445 [n=474] vs
1748 [n=477], P=0,03), mais les taux d'admission en clinique par 1 000
n'étaient pas significativement différents entre les deux
groupes (700 [n=474] vs 740 [n=477], P=0,66). Dans un groupe
prédéfini de patients à haut risque d'hospitalisation
(comprenant 112 patients d'intervention et 114 patients de soins habituels),
les taux de visites aux urgences et des admissions en clinique étaient
inférieurs chez les patients d'intervention au cours de la
deuxième année (848 [n=106] vs 1314 [n=105]; P=0,03 et 396
[n=106] vs 705 [n=105]; P=0,03, respectivement).
Conclusions Les traitements gériatriques
intégrés dispensés à domicile ont permis
d'améliorer la qualité des soins et de réduire le recours
aux soins intensifs chez des patients à haut risque. En matière
de qualité de vie liée à la santé, les
résultats furent mitigés. Quant aux comportements physiques, on
n'a pas relevé de différence entre les deux groupes. Il faudra
d'autres études pour déterminer si un ciblage plus
spécifique peut améliorer l'efficacité du programme et
si, en prescrivant moins de soins intensifs, on peut réduire les
coûts du programme.
Trial Registration
clinicaltrials.gov
Identifier: NCT00182962.
JAMA.
2007;298(22):2623-2633
Les seniors à revenus modestes représentent un groupe
divers et complexe d'adultes âgés qui subissent souvent des
facteurs tels que stress socioéconomiques, manque de connaissances
médicales, maladies chroniques et accès limité aux
soins1. En outre, ce
groupe absorbe une part disproportionnée des dépenses de
santé et, notamment, des recours aux soins
intensifs2. En
général, les adultes âgés, surtout s'ils sont
pauvres, ne reçoivent pas le niveau recommandé de soins et n'ont
souvent pas accès aux services préventifs ni à la prise
en charge des maladies chroniques et des syndromes
gériatriques3-5.
Le modèle de soins primaires GRACE (Geriatric Resources for
Assessment and Care of Elders) a été mis au point pour
améliorer la qualité des soins prodigués aux seniors
à revenus modestes. Ce modèle s'appuie sur les leçons
apprises lors d'efforts réalisés précédemment en
vue d'améliorer, par des évaluations multidimensionnelles, les
soins offerts aux adultes âgés. Un examen de cette
littérature suggère qu'une consultation gériatrique
limitée dans le temps et effectuée en un site spécifique
n'a, sur le processus et les résultats, qu'un impact
partiel6-8.
L'efficacité économique du protocole ACE (Acute Care for Elders)
a par ailleurs été démontrée. Chez des patients
âgés hospitalisés, on obtient avec ce modèle de
meilleurs résultats en confiant les soins gériatriques à
une équipe interdisciplinaire. Cette dernière permet
d'intégrer et d'améliorer les soins prodigués par les
médecins travaillant en milieux
hospitaliers9-12.
Nous inspirant de ce modèle ACE, nous avons, en développant
l'intervention GRACE, amélioré l'intégration
longitudinale des services généraux et gériatriques.
Mieux répartis dans l'ensemble des soins, ces services offrent, aux
adultes âgés, une meilleure probabilité de recevoir les
soins
recommandés13.
Comparée aux études antérieures de soins
intégrés à
domicile14-19,
l'intervention GRACE se caractérise par les avantages suivants :
évaluation et soins à domicile assurés par une
équipe constituée d'un infirmier diplômé et d'un
travailleur social ; mise en oeuvre intensive de protocoles
d'évaluation et de gestion des conditions gériatriques
habituelles ; gestion des dossiers et des traitements médicaux par
Internet ; intégration avec les services pharmaceutiques, de
psychothérapie, de soins à domicile ainsi qu'avec les services
gériatriques publics et les institutions
hospitalières13.
|
|

|
|
Figure 1.. Patients et médecins ayant participé à
l'étude
a Les 236 médecins éligibles au cours de
l'étude ont tous été randomisés et 164
médecins avaient un patient inscrit dans l'étude. Parce que
l'unité de répartition était les médecins, les
patients appartenaient déjà à un groupe lors de
l'évaluation de leur éligibilité. Cependant les patients
n'étaient assignés à un groupe qu'après leur
interview de départ et après la confirmation de prise en charge
par un médecin généraliste.
bLes patients qui n'ont pas pu être contactés sont
restés dans l'étude et ont été contactés
pour des évaluations postérieures.
|
|
|
Nous avons mené un essai contrôlé randomisé afin
de tester l'effet de l'intervention GRACE sur la santé des seniors
à revenus modestes vivant à domicile. Nous avons émis
l'hypothèse que, comparés aux soins habituels, les participants
à notre intervention bénéficieraient d'une prise en
charge de qualité supérieure de leurs affections
gériatriques et qu'il en résulterait un meilleur état de
santé, une plus grande autonomie dans les activités de vie
quotidienne et un moindre recours aux soins intensifs au cours des deux
années du suivi.
MÉTHODES
L'étude a été approuvée par le conseil
institutionnel de révision de l'Indiana University-Purdue University
d'Indianapolis. Tous les participants ainsi que les soignants ont rempli un
formulaire de consentement éclairé. Le
TABLEAU 1 décrit la
répartition des personnes au cours de l'essai.
|
|

|
|
Tableau 1.. Caractéristiques de départ des participants à
l'étudea
Abréviations: AVQ, activités de vie quotidienne ; VU, visites
aux urgences ; SCP, score composite physique ; SCM, score composite mental ;
QSP-9, Questionnaire de santé du patient ; PAR, probabilité
d'admissions répétées ; SF-36, questionnaire
abrégé des 36 éléments ; SPMSQ, Short Portable
Mental Status Questionnaire.
a Sept activités de vie quotidienne instrumentales et six
activités de base ont été utilisées. Chaque
indicateur a reçu une cote de 0 pour non, 1 pour un peu difficile, 2
pour très difficile et 3 pour requérant une aide. En
additionnant ces cotes, on a créé des scores AVQ pour
activités instrumentales et de base. Les fourchettes des scores
s'étalent de 0 à 21 et de 0 à 18, respectivement
|
|
|
Recrutement
Entre janvier 2002 et août 2004, des patients ont été
recrutés dans 6 centres de santé publics affiliés avec
les Wishard Health Services. Basé à Indianapolis dans l'Indiana,
ce consortium universitaire de santé en milieu urbain prend en charge
des patients dont les besoins médicaux sont importants. Le personnel de
cette pratique de soins primaires est constitué des professeurs et
internes de l'école universitaire de médecine. Ils soignent
environ 6 000 adultes âgés. Des patients consultant leur
médecin généraliste ont été
contactés par un chercheur adjoint formé qui les a
sélectionnés pour une participation éventuelle sur la
base des critères suivants: âgé de 65 ans ou plus, patient
reconnu (ayant consulté un généraliste à ce
même site au moins une fois dans l'année écoulée,
personne dont le revenu est de moins de 200 % du niveau fédéral
de pauvreté (ce qui, dans l'Indiana, donne droit à une assurance
Medicaid ou au plan médical du comté). Les critères
d'exclusion suivants ont notamment été retenus : personne
résidant dans une maison de soins ou cohabitant avec un participant
déjà inscrit dans cette étude, personne participant
à une autre étude ou suivant une dialyse, personne souffrant
d'un déficit auditif sévère, ne parlant pas anglais, ne
disposant pas du téléphone ou souffrant d'un déficit
cognitif sévère (score 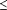 5 au SPMSQ ou Short Portable Mental
Status Questionnaire), personne ne pouvant, faute de soignant à
disposition, consentir à participer. 5 au SPMSQ ou Short Portable Mental
Status Questionnaire), personne ne pouvant, faute de soignant à
disposition, consentir à participer.
Randomisation
Afin de minimiser le potentiel de contamination entre groupes, on a pris
comme unité de randomisation les médecins
généralistes des cliniques participantes. Tous les
généralistes ont été répartis en fonction
des strates formées par leur statut d'enseignant (membre de la
faculté ou interne) et le site clinique. Le biostatisticien de
l'étude a dressé des listes de répartition à
l'aide de la méthode RNGDA (Random Number Generator for Discrete data)
de la bibliothèque de programmes
FORTRAN/IMSL21.
Aucun des médecins n'a refusé de participer. Ils ne savaient pas
à quel groupe de répartition ils appartenaient, mais certains
médecins l'ont découvert quand les chercheurs du groupe
d'intervention GRACE les ont contactés concernant un de leurs patients.
Les médecins du groupe de contrôle n'ont pas eu accès au
groupe d'intervention. Le directeur de recherche (G.D.R.) a informé les
patients de leur groupe de répartition après que ces derniers
aient donné leur consentement et rempli le questionnaire de
départ.
Intervention
L'intervention GRACE comprend un infirmier spécialisé et un
travailleur social (formant une équipe de soutien GRACE) et cette
équipe prend en charge les seniors à revenus modestes en
collaboration avec le généraliste et une équipe
interdisciplinaire conduite par un gériatre. Ces équipes de
soutien GRACE étaient assignées à des sites et à
des médecins déterminés. Au cours de
l'étude3, les
pratiques généralistes ont fait appel à ces
équipes pour la mise en œuvre des éléments
clés de l'intervention GRACE (voir encadré). Lors du
recrutement, l'équipe de soutien GRACE se rendait au domicile du
patient pour effectuer une première évaluation
gériatrique exhaustive. Ensuite, lors de la réunion hebdomadaire
suivante, l'équipe de soutien présentait ses évaluations
à l'ensemble de l'équipe interdisciplinaire GRACE en vue
d'élaborer un programme thérapeutique personnalisé. Ce
programme comprenait la mise en oeuvre des protocoles GRACE ainsi que les
suggestions formulées par l'équipe pour l'évaluation et
la gestion des conditions gériatriques habituelles. Munie de ce
programme thérapeutique, l'équipe de soutien GRACE rencontrait
face à face le médecin généraliste du patient afin
de réviser et modifier le programme avec lui. Avec l'appui du
généraliste et de l'équipe interdisciplinaire,
l'équipe de soutien GRACE passait alors à la mise en oeuvre du
programme en respectant les objectifs du patient. L'équipe rencontrait
ce dernier (habituellement à son domicile ou, parfois, au bureau,
à l'hôpital ou à la maison de soins). Grâce à
des entretiens téléphoniques l'équipe restait en contact
avec le patient, les membres de sa famille, les soignants et les
professionnels des soins de santé. Afin d'évaluer la mise en
oeuvre du programme, chaque patient a reçu au minimum une visite de
suivi à domicile, un appel téléphonique ou une rencontre
en tête à tête par mois. Après chaque visite aux
urgences ou chaque hospitalisation, une rencontre en tête à
tête était prévue au domicile du patient. Pour le reste,
le nombre, la périodicité et le contenu des autres rencontres
avec le patient étaient dictés par la mise en oeuvre du
programme thérapeutique. Chaque année, le cycle était
relancé par une réévaluation à domicile. Une
description détaillée du modèle GRACE a été
publiée
antérieurement13.
Et les protocoles GRACE sont disponibles sur
http://iucar.iu.edu/research/graceteamsuggestions.pdf.
Les patients du groupe de contrôle ont eu accès à tous
les services de soins primaires et spécialisés habituellement
disponibles. Au moment de l'intervention GRACE, les services
gériatriques suivants étaient proposés au centre Wishard
dans le cadre des pratiques généralistes : centre
d'évaluation gériatrique offrant des spécialités
multiples aux patients externes, unité ACE et service de consultation
pour patients hospitalisés, soins hospitaliers
spécialisés et visites médicales à domicile. Le
centre public de santé mentale offrait également des soins
psychiatriques.
| Encadré. Éléments clés de l'intervention
« Geriatric Resources for Assessment and Care of Elders »
(GRACE)a
Évaluation gériatrique exhaustive initiale et annuelle
effectuée à domicile par une équipe de soutien comprenant
un infirmier diplômé et un travailleur social
Chaque année, un programme de soins personnalisé est
élaboré par l'équipe de soutien GRACE avec l'aide de
l'équipe gériatrique interdisciplinaire qui réunit un
gériatre, un pharmacien, un kinésithérapeute, un
psychologue social et un représentant des services à
domicile.
Réactivation annuelle des protocoles GRACE et des suggestions de
l'équipe concernant les 12 conditions gériatriques visées
: planification avancée des soins, maintien de la santé, gestion
des médicaments, difficultés motrices/chutes, douleur chronique,
incontinence, dépression, perte auditive, déficience visuelle,
malnutrition ou perte de poids, démence et charge pour le soignant.
L'équipe de soutien GRACE rencontre le médecin
généraliste du patient et examine, modifie et organise avec lui
la planification initiale et annuelle des protocoles ainsi que les suggestions
de l'équipe.
Mise en oeuvre par l'équipe de soutien du programme des soins et des
suggestions de l'équipe en collaboration avec le médecin
généraliste et dans la ligne des objectifs du patient.
Réunions hebdomadaires de l'équipe interdisciplinaire GRACE
afin d'évaluer les succès de l'équipe de soutien dans la
mise en oeuvre des protocoles et afin de surmonter les obstacles
rencontrés.
Gestion par l'équipe de soutien GRACE des soins à domicile
(notamment des contacts mensuels avec le patient) à l'aide d'un
réseau médical électronique et d'une application Web de
traçage, ce qui permet de coordonner les soins et d'assurer leur
continuité entre tous les professionnels et tous les sites de la
santé.
aGRACE signifie Geriatric Resources for Assessment and Care of
Elders.
|
|
Critères de jugement
Les participants ont rempli des évaluations de départ ainsi
qu'au 6e, 12e, 18e et 24e mois. Ces évaluations
téléphoniques ont été menées par des
intervieweurs qui ne connaissaient pas le groupe de répartition des
patients et qui n'avaient participé ni au recrutement ni à
l'intervention. Les critères de race et d'ethnicité ont
été retenus parce qu'ils peuvent, en tant que variables
indépendantes, représenter des facteurs potentiellement
importants pour la détermination de l'efficacité de
l'intervention GRACE. Les patients identifiaient eux-mêmes leur race et
leur ethnicité pour les intervieweurs en se basant sur une liste
d'options prédéterminées établie par l'Institut
national de la santé. Pour mesurer la sévérité des
dépressions, on a utilisé le questionnaire-9 d'état de
santé du
patient22. Les
données de santé relatives au processus de mise en oeuvre de
l'intervention GRACE ont été recueillies via un système
de traçage par Internet spécifiquement conçu pour ce
projet.
Pour évaluer la qualité des traitements médicaux, nous
avons utilisé les indicateurs de qualité ACOVE (Assessing Care
of Vulnerable Elders) spécifiquement développés pour
évaluer l'ensemble des soins prodigués aux personnes
âgées vulnérables, dont les « syndromes
gériatriques
»23-25.
Il existe une association étroite entre de meilleurs indicateurs de
qualité ACOVE et les taux de survie plus élevés parmi les
adultes âgés vulnérables vivant à
domicile26. Nous
avons choisi les indicateurs de qualité ACOVE qui évaluent
spécifiquement les conditions gériatriques ciblées par
l'intervention GRACE et que rendaient disponibles les dossiers médicaux
électroniques ou les interviews des patients.
Parmi les critères de jugement figuraient: les échelles et
évaluations médicales spécifiées dans le
questionnaire des 36 éléments (SF-36) ; les activités de
vie quotidienne (AVQ) instrumentales et de base, les visites aux urgences et
les hospitalisations. Pour évaluer la qualité de vie liée
à la santé des patients, nous avons utilisé huit
éléments de la liste SF-36 (fonctionnement physique, limitations
dues à l'état physique, douleur physique, état de
santé général, vitalité, fonctionnement social,
état psychique et santé
mentale)27. Ces
éléments ont été assemblés en un score
composite physique (PCS pour Physical Component Summary) et un score composite
mental (MCS pour Mental Component
Summary)28. Il a
été démontré que les variations intergroupes qui,
sur une échelle de 0 à 100, atteignent 2 points ou plus
représentent une différence cliniquement ou socialement
significative29.
Pour évaluer l'état AVQ des patients, nous avons utilisé
les critères de l'enquête AHEAD (Assets and Health Dynamics of
the
Oldest-Old)30.
De la grille AVQ, mous avons retenu sept activités instrumentales et
six activités de base et chacune de ces activités a reçu
une cote de 0 point pour non, 1 pour un peu difficile, 2 pour très
difficile et 3 pour requérant une aide. En additionnant ces cotes, on a
créé des scores AVQ pour activités instrumentales et de
base. Les fourchettes des scores s'étalent de 0 à 21 et de 0
à 18, respectivement pour ces deux types d'activité. On a
également relevé les journées passées au lit
à la suite d'une maladie ou d'une blessure au cours des 6 mois
antérieurs (plus d'un demi-jour) en dehors des séjours à
l'hôpital ou en maison de soins. La satisfaction des patients quant aux
soins prodigués a été évaluée comme suit :
excellente, très bonne, bonne, acceptable ou pauvre.
En assumant un taux d'usure de 20 %, nous avons estimé qu'un
échantillon de 500 patients par groupe nous fournirait 80 % de la
puissance nécessaire pour détecter les variations
significatives: soit un effet standard de 0,26 pour les déviations de
la grille SF-36 et un niveau de signification de 0,05 pour la grille
AVQ31. En raison
des limitations de nos ressources, le recrutement a été
interrompu avant que la cible de 1 000 nouveaux patients ait été
atteinte, mais, pour la grille SF-36, la taille d'effet a été
plus importante que prévu si bien que nous disposions d'une puissance
suffisante pour détecter une différence statistiquement
significative.
Pour comptabiliser les visites aux urgences, les admissions en clinique et
les séjours hospitaliers, nous avons obtenu les données du
réseau de santé local qui gère les 5 principaux
hôpitaux d'Indianapolis. Dans nos statistiques des visites aux urgences,
les visites ayant abouti à une hospitalisation ne sont pas incluses
parce que ces épisodes de soins intensifs apparaissent dans les
statistiques d'hospitalisation. Les risques d'hospitalisation ne figurant pas
parmi les critères de recrutement, nous avons aussi calculé la
probabilité des admissions répétées (PAR) de
chaque patient en fonction des facteurs suivants : âge, sexe,
état de santé perçu, présence d'un soignant
informel, condition cardiaque, diabète, visites d'un médecin et
hospitalisations32.
Lors de la planification de notre stratégie, nous avons estimé
qu'à partir d'un indice PAR de 0,4 ou plus, un risque
élevé d'hospitalisation se
présentait33
et nous avons, au même titre que l'échantillon complet, inscrit
ce groupe de patients dans notre analyse des recours aux soins intensifs.
Analyse statistique
Les comparaisons intergroupes sont basées sur les tests t pour les
variables continues et sur les tests  2 pour les variables
catégorielles. Pour les grilles SF-36 et AVQ, nous avons utilisé
des modèles régressifs afin d'évaluer l'effet de
l'intervention en intention de traiter sur les variations des critères
entre la ligne de départ et le 24e
mois34. Ces
modèles sont de nature hiérarchique, car ils intègrent,
dans une structure nichée, les effets de chaque patient sur chaque
médecin et les effets de chaque médecin sur chaque
consultation35. Les
groupes de traitement ont examiné les amplitudes et
périodicités des données manquantes et comparé
celles-ci entre les groupes. Pendant le suivi, nous avons, pour estimer les
résultats manquants, utilisé la méthode de la
dernière observation rapportée (LOCF). Afin d'évaluer les
résultats fournis par ces deux méthodes d'estimation, nous avons
répété nos analyses de tous les critères
principaux en utilisant la méthode d'estimation par régression
multiple36. Les
résultats ne différant pas d'une méthode d'estimation
à l'autre, nous avons donc rapporté les données obtenues
par la méthode LOCF. Deux facteurs caractérisent le recours aux
soins intensifs: les visites aux urgences et les admissions en clinique. Pour
comptabiliser ces deux facteurs, nous avons utilisé les modèles
de régression log-linéaire. En raison des désistements
précoces, les durées des périodes de suivi sont
inégales. En conséquence, nous avons ajusté notre
modèle log-linéaire en lui intégrant en tant que
paramètre d'ajustement le logarithme de durée. Le modèle
nous a fourni les paramètres de régression et les erreurs. Quant
aux ratios du taux d'incidence de l'effet du traitement, nous les avons
obtenus en élevant à la puissance les estimations du
paramètre de régression, ce qui a été fait tant
pour les visites aux urgences que pour les admissions en clinique. Pour en
faciliter l'interprétation, nous avons rapporté les taux annuels
de visites et d'admissions par 1 000 participants. Les taux de
mortalité ont été analysés à l'aide des
tests 2 pour les variables
catégorielles. Pour les grilles SF-36 et AVQ, nous avons utilisé
des modèles régressifs afin d'évaluer l'effet de
l'intervention en intention de traiter sur les variations des critères
entre la ligne de départ et le 24e
mois34. Ces
modèles sont de nature hiérarchique, car ils intègrent,
dans une structure nichée, les effets de chaque patient sur chaque
médecin et les effets de chaque médecin sur chaque
consultation35. Les
groupes de traitement ont examiné les amplitudes et
périodicités des données manquantes et comparé
celles-ci entre les groupes. Pendant le suivi, nous avons, pour estimer les
résultats manquants, utilisé la méthode de la
dernière observation rapportée (LOCF). Afin d'évaluer les
résultats fournis par ces deux méthodes d'estimation, nous avons
répété nos analyses de tous les critères
principaux en utilisant la méthode d'estimation par régression
multiple36. Les
résultats ne différant pas d'une méthode d'estimation
à l'autre, nous avons donc rapporté les données obtenues
par la méthode LOCF. Deux facteurs caractérisent le recours aux
soins intensifs: les visites aux urgences et les admissions en clinique. Pour
comptabiliser ces deux facteurs, nous avons utilisé les modèles
de régression log-linéaire. En raison des désistements
précoces, les durées des périodes de suivi sont
inégales. En conséquence, nous avons ajusté notre
modèle log-linéaire en lui intégrant en tant que
paramètre d'ajustement le logarithme de durée. Le modèle
nous a fourni les paramètres de régression et les erreurs. Quant
aux ratios du taux d'incidence de l'effet du traitement, nous les avons
obtenus en élevant à la puissance les estimations du
paramètre de régression, ce qui a été fait tant
pour les visites aux urgences que pour les admissions en clinique. Pour en
faciliter l'interprétation, nous avons rapporté les taux annuels
de visites et d'admissions par 1 000 participants. Les taux de
mortalité ont été analysés à l'aide des
tests  2. La durée entre le recrutement et le décès a
été examinée à l'aide des estimations de
Kaplan-Meier basées sur les courbes de survie et comparée
à l'aide du test de Wilcoxon. Pour toutes les analyses, nous avons
utilisé la version 9.1 du logiciel SAS de SAS Institute Inc de Cary en
Caroline du Nord. Nous avons estimé qu'à partir de P<0,05,
les tests deviennent significatifs. 2. La durée entre le recrutement et le décès a
été examinée à l'aide des estimations de
Kaplan-Meier basées sur les courbes de survie et comparée
à l'aide du test de Wilcoxon. Pour toutes les analyses, nous avons
utilisé la version 9.1 du logiciel SAS de SAS Institute Inc de Cary en
Caroline du Nord. Nous avons estimé qu'à partir de P<0,05,
les tests deviennent significatifs.
RÉSULTATS
Caractéristiques de l'échantillon
Le TABLEAU 1 montre les
caractéristiques de départ des 951 patients randomisés
entre le groupe d'intervention et le groupe de soins habituels. Ces patients
ont été pris en charge par 164 médecins
généralistes différents (78 dans le groupe d'intervention
et 86 dans le groupe des soins habituels). Pour les médecins femmes,
les proportions entre les deux groupes sont similaires: 42 % vs 36 % ; P=0,41.
Entre les spécialistes de médecine interne et les
spécialistes de médecine interne/pédiatrie, les
proportions sont de 72 % vs 73 % ; P=0,83. Entre le centre de santé
principal et l'un des cinq centres publics de santé, elles sont de 49 %
vs 50 %; P=0,87. L'écart du nombre de patients par médecin va de
1 à 49 (moyenne de 3) dans le groupe d'intervention et de 1 à 63
(moyenne de 2) dans le groupe des soins habituels. Les professeurs de
faculté ont pris en charge environ 80 % des patients du groupe
d'intervention et 75 % des patients du groupe des soins habituels (P=0,07).
Conformément au profil de l'échantillon ciblé, trois
quarts des patients de l'étude sont des femmes, plus de la
moitié sont noirs et tous sont de condition socioéconomique
désavantagée. Dans les deux groupes, la plupart des patients
peuvent, de manière autonome indépendante, exécuter les
activités instrumentales (64 % vs 62 % ; P=0,45) et les
activités de base (83 % vs 87 %; P=0,11) de la vie quotidienne. La
plupart des patients souffrent de multiples pathologies co-morbides et
gériatriques et affichent un taux élevé de recours aux
soins intensifs. Presque 1 sur 4 des participants présente un risque
élevé d'hospitalisation ayant un score RPA de 0,04 ou plus (112
dans le groupe d'intervention et 114 dans le groupe des soins habituels).
Soins reçus par les patients du groupe d'intervention GRACE
Le TABLEAU 2 montre le
processus des soins et la mise en oeuvre des éléments
clés de l'intervention GRACE. Après une évaluation
clinique de départ, l'équipe de soutien GRACE a suivi les
patients de ce groupe pendant la première année (n=447). Elle a
effectué alors une évaluation annuelle et a continué
à suivre les patients pendant la deuxième année (n=409).
D'une année à l'autre, on remarque que le nombre des patients
diminue à cause des décès, des
déménagements et des désistements de patients. Le nombre
des patients pris en charge par l'équipe de soutien GRACE ne correspond
donc pas nécessairement avec le nombre (affiché dans le
tableau 1) des patients
contactés par les intervieweurs de l'étude. Les patients du
groupe d'intervention ont, en moyenne, été contactés 18
fois au cours de la première année (fourchette de 1 à 65)
et 17 fois au cours de la deuxième année (fourchette de 1
à 90). Un tiers de ces contacts sont des rencontres en tête
à tête (habituellement au domicile du patient) et deux-tiers des
contacts téléphoniques.
|
|

|
|
Tableau 2.. Processus de soins des patients de l'intervention GRACEa
Abréviation: GRACE, Geriatric Resources for Assessment and Care of
Elders.
a Les chiffres de l'an 1 (n = 447) représentent les
patients de l'intervention GRACE ayant subi l'évaluation clinique
initiale et dont les dossiers complets figurent dans le système Web de
traçage pour l'an 1 tandis que les chiffres de l'an 2 (n = 409)
représentent les patients de l'intervention GRACE ayant subi
l'évaluation clinique initiale et dont les dossiers complets figurent
dans le système Web de traçage pour l'an 2.
b Les contacts face à face avec le patient se sont
déroulés habituellement au domicile du patient, mais parfois
aussi au bureau, à l'hôpital ou à la maison de
santé. Les chiffres ayant été arrondis, leur somme n'est
pas égale à 100.
|
|
|
Qualité des soins médicaux
En ce qui concerne les affections gériatriques et les processus de
soins ciblés par l'intervention GRACE, le
TABLEAU 3 compare
l'adhésion aux indicateurs de qualité ACOVE dans le groupe
d'intervention et dans le groupe des soins habituels. On relève, chez
les patients du groupe d'intervention affichant des syndromes
gériatriques, une plus grande probabilité de voir leurs dossiers
médicaux électroniques renseigner ces syndromes. Ces patients
rapportent également que leurs affections ont été
identifiées ou ont fait l'objet d'un diagnostic et qu'ils ont
reçu une consultation spécialisée ainsi que des
informations et un traitement approprié. Enfin, les patients
eux-mêmes ou leurs dossiers rapportent une meilleure adhésion aux
indicateurs de qualité mesurant les soins préventifs, la
continuité des soins, la prise des médicaments et les soins
palliatifs.
|
|

|
|
Tableau 3.. Qualité des soins médicaux au cours de l'an 1
Abréviation : PHQ-9, Patient Health Questionnaire-9.
|
|
|
Résultats thérapeutiques
Le TABLEAU 4 affiche les
résultats thérapeutiques relatifs aux grilles SF-36 et AVQ. Les
coefficients reflètent les différences entre le groupe
d'intervention et le groupe des soins habituels en calculant la moyenne des
changements détectés au cours des 2 années. On
relève, dans le groupe d'intervention, des scores significativement
meilleurs pour 4 des 8 éléments de la grille SF-36 (état
de santé général, vitalité, comportement social et
santé mentale) ainsi que pour le score composite mental (MCS). Pour les
changements AVQ, on n'observe pas de différence de moyenne à 2
ans et l'analyse des scores regroupés en catégories de meilleur,
équivalent ou pire a confirmé ces résultats. On ne
relève pas de différence significative non plus dans la
catégorie « requérant de l'aide » entre les scores
de départ et ceux du 24e mois en ce qui concerne les AVQ instrumentales
(21 % vs 24 %; P=0,25) et de base (12 % vs 13 %; P=0,64). À 24 mois, 64
% des patients du groupe d'intervention s'estiment très ou pleinement
satisfaits des soins reçus comparé à 63 % pour les
patients du groupe des soins habituels (P=0,31). Autres similarités
entre les groupes: les taux de mortalité à 24 mois (33 pour le
groupe d'intervention [7,0 %] vs 37 pour le groupe des soins habituels [7,8
%]; P=0,64) et la survenue des décès.
|
|

|
|
Tableau 4.. Valeurs de départ et impact du traitement sur les résultats
thérapeutiques par groupe d'étude a
Abréviations : AVQ, activités de vie quotidienne ; SCP, score
composite physique ; SCM, score composite mental ; SF-36, questionnaire
abrégé des 36 éléments.
a Des scores SF-36 plus élevés représentent
une meilleure santé alors que des scores AVQ plus élevés
représentent plus de difficultés ou une plus grande
dépendance.
b Les valeurs affichées sont les valeurs P pour l'effet
du traitement.
|
|
|
Recours aux services de soins intensifs
Nous avons d'abord examiné les différences entre les taux
relevés dans l'ensemble de l'échantillon et, ensuite, chez les
patients présentant un risque élevé d'hospitalisation
selon leur probabilité d'admissions
répétées(32,33).
Le TABLEAU 2 affiche les
visites aux urgences (non associées à une admission en clinique)
et les hospitalisations pour le groupe d'intervention et le groupe des soins
habituels au cours des 24 mois de l'étude. Le taux cumulé des
visites aux urgences par 1 000 est inférieur dans le groupe
d'intervention (1445 [n=474] vs 1748 [n=477]; P=0,03). Entre les deux groupes,
on remarque que les taux de visites aux urgences par 1 000 sont similaires au
cours de l'an 1 (823 [n=474] vs 937 [n=477] ; P=0,22), mais qu'au cours de
l'an 2, les taux du groupe d'intervention sont significativement
inférieurs (643 [n=459] vs 841 [n=460] ; P=0,01). À 2 ans, les
taux intergroupes cumulés par 1 000 ne diffèrent ni pour les
admissions en cliniques (700 [n=474] vs 740 [n=477] ; P=0,66) ni pour les
séjours hospitaliers (3759 [n = 474] vs 4069 [n = 477]; P=0,66). On ne
relève pas de différence significative entre groupe
d'intervention et groupe de soins habituels pour les admissions et les
séjours hospitaliers par 1 000 ni au cours de l'an 1 (384 [n=474] vs
358 [n=477] admissions par 1 000 ; P=0,66 et 2076 [n=474] vs 1983 [n=477]
journées par 1000 ; P=0,85) ni au cours de l'an 2 (325 [n=459] vs 396
[n=460] admissions par 1 000 ; P=0,22 et 1739 [n=459] vs 2163 [n=460]
journées par 1 000; P=0,37). Pas de différence significative non
plus entre les groupes dans la proportion des patients hospitalisés
réadmis dans les 30 jours après leur sortie de l'hôpital
(26 % [n = 206] vs 32 % [n = 200]; P=0,24).
Le tableau 2 montre
également les taux de visites aux urgences et les taux d'admissions en
clinique des patients qui présentaient au départ un risque
élevé d'hospitalisation (score RPA de 0,04 ou plus, soit 112
patients dans le groupe d'intervention et 114 dans le groupe des soins
habituels). Au cours de l'an 1, les taux d'admissions et de séjours
hospitaliers par 1 000 sont similaires entre les groupes d'intervention et de
soins habituels chez ces patients à haut risque (705 [n = 112] vs 798
[n=114] admissions par 1000 ; P=0,60 et 3938 [n=112] vs 4544 [n=114]
journées par 1 000 ; P=0,68). Cependant, au cours de l'an 2, les taux
d'admissions en clinique sont significativement inférieurs pour les
patients du groupe d'intervention (396 [n=106] vs 705 [n=105] ; P=0,03) alors
que, pour les séjours hospitaliers, les différences ne sont
statistiquement pas significatives (2152 [n=106] vs 3943 [n=105] ; P=0,13). De
même, les visites aux urgences sont significativement inférieures
pour le groupe d'intervention au cours de l'an 2 (848 [n=106] vs 1314 [n=105]
; P=0,03), mais pas au cours de l'an 1 (1098 [n=112] vs 1149 [n=114] ;
P=0,79).
|
|

|
|
Figure 2.. Recours aux soins intensifs au départ et pendant les 2 années
de suivi par groupe d'étude
Les barres d'erreur représentent les 95 % d'intervalle de confiance.
Les taux des visites aux urgences ne comprennent pas les visites
associées aux admissions en clinique.
|
|
|
COMMENTAIRES
Ceci est, à notre connaissance, le plus important essai clinique
randomisé visant à évaluer, dans le cadre d'un
système de santé, une intervention gériatrique
conçue pour améliorer les traitements de seniors aux revenus
modestes vivant à domicile. Dans l'élaboration du protocole,
nous avons spécifiquement voulu examiner le processus des soins et
mesurer un vaste éventail de critères qu'adultes
âgés et responsables de systèmes de santé
trouveront importants. Les résultats comprennent des critères
relatifs, non seulement et entre autres, aux comportements et aux traitements
qui déterminent la qualité de vie, mais aussi aux
procédures thérapeutiques les plus coûteuses. Les
pratiques de médecine générale impliquées dans
cette étude soignent une population multiraciale de seniors pauvres,
souffrant de multiples comorbidités et dont les traitements sont
souvent répartis entre divers prestataires et centres de soins. Lors
d'essais précédents, on a fait peu de cas de ces groupes de
patients qui représentent une population complexe dont la prise en
charge s'avère onéreuse. Ces patients pourraient cependant tirer
le plus grand profit d'une meilleure coordination et intégration de
leurs traitements. Nos conclusions sont les suivantes : comparé au
groupe des soins habituels, les patients de l'intervention GRACE ont
reçu des traitements de meilleure qualité et leurs indicateurs
de qualité de vie liés à la santé se sont
significativement améliorés. Nous n'avons pas relevé de
différence significative quant aux critères traditionnels des
fonctions gériatriques. Au cours des deux années de suivi, les
patients du groupe d'intervention ont effectué moins de visites aux
urgences. En outre, parmi le groupe présentant un risque
élevé d'hospitalisation répétée, le nombre
des admissions en clinique a diminué au cours de la deuxième
année.
Nous avons élaboré le protocole pour patients externes de
l'intervention GRACE en nous basant sur son prédécesseur : le
modèle
ACE10,12,37
conçu pour patients internes.
L'approche adoptée par les deux modèles consiste à
compléter et soutenir le rôle du médecin
généraliste en aidant celui-ci à identifier des
conditions gériatriques fréquentes, mais souvent non reconnues.
L'intervention GRACE fournit des ressources permettant d'évaluer et de
traiter ces patients. Grâce à une étroite collaboration
tant avec le médecin généraliste qu'avec les cliniciens
hospitaliers, nous avons pu tirer parti des ressources limitées
offertes par les gériatres formés et les équipes
gériatriques multidisciplinaires pour avoir un énorme impact sur
les résultats thérapeutiques. À la différence des
essais antérieurs qui se sont penchés surtout sur l'ensemble des
traitements gériatriques administrés à domicile
indépendamment ou en parallèle avec des prestataires de soins
primaires38,
39, l'intervention GRACE
s'est pleinement intégrée aux pratiques de soins primaires. Les
équipes de soutien GRACE étaient au service des pratiques de
soins primaires et assignées à des centres et à des
médecins spécifiques. En outre, les protocoles GRACE ainsi que
les rôles de l'infirmier diplômé et du travailleur social
ont été définis en harmonie avec les pratiques de soins
primaires.
La qualité des traitements prodigués aux patients
âgés vivant à domicile n'atteint pas des niveaux
acceptables en raison d'une variété de conditions et, notamment,
de conditions influençant uniquement la santé des patients
gériatriques5.
On a démontré qu'il existe une corrélation entre la
qualité des traitements gériatriques telle que la mesurent les
indicateurs ACOVE et la
mortalité26.
En utilisant les indicateurs ACOVE développés
spécifiquement pour mesurer les principaux facteurs auxquels sont
exposées les personnes âgées vulnérables, nous
avons trouvé que, comparée aux soins habituels, l'intervention
GRACE améliore substantiellement la qualité des traitements des
conditions gériatriques et des soins primaires ciblés.
Cependant, les meilleurs taux des diagnostics posés pour les conditions
gériatriques peuvent, dans le groupe d'intervention, partiellement
s'expliquer par la meilleure gestion des dossiers médicaux
électroniques que tenaient à jour les médecins ainsi que
par les soins avancés confiés aux équipes de soutien
GRACE.
Á l'instar d'autres interventions multi facettes récentes,
l'intervention GRACE n'a pas abouti à améliorer les
critères de santé physique. Les questionnaires SF-36
enregistrent des progrès, mais ceux-ci restent inconsistants et d'une
amplitude suffisamment faible que pour mettre en question leur
significativité clinique. La présente étude est cependant
la première intervention à domicile à rapporter des
améliorations des échelles SF-36 chez des adultes
âgés en phase non terminale. Un essai de médecine
générale à domicile mené par une équipe des
Veterans Affairs rapporte des progrès significatifs à 12 mois
chez des patients en phase terminale dans six des huit échelles SF-36
(toutes les échelles sauf le fonctionnement physique et le
fonctionnement de rôle), mais pas de différences en faveur de
l'intervention chez des patients en phase non terminale atteints d'une
invalidité
sévère16.
Rapportée récemment, une évaluation exhaustive de
patients gériatriques
externes31 a
relevé des résultats positifs à 15 mois pour les
échelles SF-36 de fonctionnement physique, vitalité,
comportement social et score composite physique. Cette évaluation
s'accompagnait de stratégies développées pour une
meilleure adhésion aux recommandations de soins. Dans une étude
multicentre de l'administration des anciens combattants (VA), des patients
âgés vulnérables et hospitalisés ont reçu,
après leur sortie d'hôpital, un suivi et une évaluation
externes qui, à 12 mois, ont relevé des progrès
uniquement dans l'échelle SF-36 de santé
mentalê40. Il
se peut qu'il ne soit pas facile d'interpréter les changements
détectés dans les échelles
SF-3641,
42. Mais l'amplitude des
variations de l'intervention GRACE va de 5 à 10 %, ce qui correspond
aux variations rapportées par les trois études
mentionnées ci-dessus.
Parmi les raisons expliquant pourquoi le modèle GRACE n'a pas
amélioré plus efficacement les résultats
thérapeutiques, citons une déficience de la stratégie de
ciblage des patients présentant un risque de déclin. Dans le
groupe de soins habituels, la moyenne sur 2 ans du déclin a
été de seulement 2,4 pour les échelles SF-36. En outre,
les patients de ce groupe ont reçu des éléments de
l'intervention GRACE quand ils ont consulté des services
gériatriques spécialisés. Au cours de la présente
étude, 2,1 % des patients de l'intervention et 1,5 % des patients des
soins habituels (P=0,45) ont été vus par le médecin du
programme des soins à domicile, 4 % des patients de chaque groupe ont
été vus par le centre des évaluations gériatriques
externes et 18 % des patients d'intervention vs 11 % des patients des soins
habituels (P=0,003) ont été vus par le service de consultation
interne ACE.
L'intervention GRACE comprend des évaluations gériatriques
multidimensionnelles et de multiples visites de suivi à domicile.
Pourtant, nous ne relevons pas de preuves d'une amélioration des
activités de vie quotidienne (AVQ) ni d'une prévention d'un
déclin de ces activités alors que certains autres programmes en
attestent15,38,39.
Pour cette étude, nous n'avons pas spécialement recruté
des adultes âgés ayant des difficultés à
exécuter ces activités. En fait, la plupart des participants
exécutaient de manière autonome des activités de vie
quotidienne instrumentales et de base au départ de l'étude.
À deux ans, ils continuaient à pouvoir le faire. Des
études antérieures sont parvenues à prévenir
efficacement un déclin des activités de vie quotidienne. En
contraste, la population de notre étude était plus jeune, plus
pauvre, moins éduquée et plus autonome dans ces
activités. En outre, la présente étude n'a duré
que deux ans. Une période d'intervention plus longue ou plus intense
peut être nécessaire pour améliorer les AVQ. Il se peut
aussi que nos évaluations n'aient pas détecté des
changements importants des AVQ dans cette cohorte d'adultes âgés.
Prévenir un déclin des AVQ peut nécessiter un programme
plus intensif tel qu'une physiothérapie à domicile axée
principalement sur l'amélioration des déficiences sous-jacentes
des capacités
physique43.
De nombreuses études d'évaluations gériatriques de
patients externes et de traitements à domicile ne parviennent pas
à démontrer une réduction des taux de recours aux soins
intensifs16-19,
38,
40,
44,
45. Cependant, des
études antérieures réussies et le présent essai
prouvent que visites aux urgences et hospitalisations diminuent quand une
équipe gériatrique interdisciplinaire assure la gestion des
soins (y compris, en général, les visites à domicile) et
travaille en étroite collaboration avec le médecin
généraliste qu'elle
soutient15,
46-49.
Avant que les taux d'utilisation ne diminuent, il se peut qu'une «
période de mise en route » soit
nécessaire47,
49. Nous avons
relevé un certain décalage avant que l'équipe de soutien
ne développe une relation de confiance avec le patient et le
médecin traitant. Peut-être cela explique-t-il pourquoi la
réduction des taux de recours aux soins intensifs se manifeste plus au
cours de la deuxième année de l'intervention GRACE. La
présente étude comporte plusieurs limitations qu'il convient de
mentionner spécifiquement. Il se pourrait que les résultats de
cette étude ne soient pas généralisables ni applicables
à d'autres groupes de personnes âgées (p.ex. des personnes
socioéconomiquement plus favorisées ou vivant en milieu rural)
ou à des centres hospitaliers différents. Étant
donné la nature de l'intervention, les médecins, l'équipe
d'intervention et les patients n'y ont pas participé en aveugle. Les
assistants de recherche ont évalué de manière
indépendante et en aveugle les résultats. Nous n'avons pas
prévu de groupe de contrôle qui n'aurait reçu que des
contacts sporadiques. De ce fait, nous ne pouvons déterminer si
l'impact de l'intervention est dû simplement aux contacts sociaux ou
pas.
On ne connaît pas l'exactitude de la base contenant les
données médicales échangées dans la région,
mais les erreurs qu'elle pourrait contenir devraient se retrouver dans les
deux groupes d'intervention et de contrôle. Pour évaluer les
principaux résultats, nous avons utilisé de multiples mesures
qui sont compatibles avec nos hypothèses originales concernant l'impact
de l'intervention et compatibles avec les meilleures pratiques de la recherche
gériatrique(50).
Pour évaluer exhaustivement les résultats, nous avons
testé des hypothèses multiples. Bien que la dynamique de la
présente étude ne permette pas de l'ajuster correctement
à des résultats multiples, nous avons
répété notre analyse des 14 critères principaux en
appliquant la correction classique de
Bonferroni(51). Les
résultats sont restés significatifs pour les échelles
SF-36 de vitalité (P=0,006), santé mentale (P=0,03) et le score
composite mental (P=0,008), mais pas pour les visites aux urgences
(P=0,42).
Dans le centre utilisé pour la présente étude, on a
également déployé avec succès des modèles
collaboratifs de soins primaires conçus pour prendre en charge la
dépression et la
démence52,53.
Les conclusions de l'intervention GRACE s'appuient sur ces approches ciblant
des traitements bien circonscrits pour explorer l'état de santé
général des patients âgés, sans négliger ces
conditions gériatriques
débilitantes54.
Nous avons trouvé que le modèle de médecine
générale GRACE peut être appliqué dans un
système public de santé prenant en charge des seniors aux
revenus modestes et que ce modèle améliore efficacement la
qualité des soins. Dans l'essai GRACE, une meilleure reconnaissance et
un meilleur traitement de la dépression contribuent au meilleur score
composite mental relevé dans le groupe d'intervention. De la même
manière, d'autres traitements améliorés ayant un effet
positif sur l'ensemble de l'état de santé peuvent réduire
le recours aux soins intensifs. Sur les fondements du modèle GRACE, on
peut efficacement et en les intégrant à la médecine
générale appliquer aux personnes âgées des
protocoles spécifiquement conçus pour les conditions
gériatriques et la gestion des maladies.
De futures études devraient comparer aux coûts des programmes
actuels les économies réalisées par un moindre recours
aux soins intensifs, et ce, afin de déterminer la faisabilité.
Sous le régime Medicare actuel de rémunération à
l'acte, la plupart des services proposés par l'intervention GRACE ne
sont pas remboursés. Toutefois, le régime Medicare de soins
intégrés présente une structure financière qui
pourrait dès à présent prendre en charge l'intervention
GRACE. Dans une structure de soins intégrés, les coûts du
modèle GRACE pourraient être compensés en partie par la
prévention du recours aux soins intensifs, une évaluation plus
judicieuse du risque grâce à une meilleure reconnaissance des
conditions médicales et des indicateurs de qualité
améliorés grâce à des traitements plus performants.
L'intervention GRACE pourrait aussi être financée par les
méthodes de remboursement proposées récemment: « un
remboursement complet pour un traitement complet ». Il s'agit d'un
remboursement ajusté aux besoins et basé sur la performance. Ou
encore par le modèle avancé des soins à
domicile55,56.
Nous espérons que le modèle GRACE deviendra, pour notre
système de santé, une innovation pratique qui contribuera
à améliorer les soins gériatriques et les
résultats tout en réduisant les recours onéreux aux soins
intensifs pour les seniors à revenus modestes.
Informations sur les auteurs
Correspondance : Steven R. Counsell, MD, Indiana University School of
Medicine, 1001 W 10th St, WOP-M200, Indianapolis, IN 46202
(scounsel{at}iupui.edu).
Contributions des auteurs: Les docteurs Counsell et Callahan ont eu
un accès illimité à toutes les données de
l'étude et assument la responsabilité de
l'intégrité des données et de l'exactitude de l'analyse
des données.
Conception et schéma de l'étude: Counsell, Callahan,
Clark, Buttar.
Acquisition des données: Counsell, Callahan, Buttar,
Ricketts.
Analyse et interprétation des données: Counsell,
Callahan, Clark, Tu, Buttar, Stump, Ricketts.
Rédaction du manuscrit: Counsell, Callahan, Tu,
Ricketts.
Revue critique du manuscrit: Counsell, Callahan, Clark, Tu,
Buttar, Stump, Ricketts.
Analyse statistique: Callahan, Tu, Stump.
Obtention des fonds: Counsell, Callahan, Buttar.
Aide administrative, technique et matérielle: Counsell,
Callahan, Buttar, Ricketts.
Supervision de l'étude: Counsell, Callahan, Buttar,
Ricketts.
Liens financiers: Les auteurs détiennent les droits sur les
protocoles et le manuel de formation. Ils peuvent vendre ces documents
à des organismes de santé intéressés qui les
utiliseront dans la gestion des traitements destinés aux patients
gériatriques, mais aucun plan n'est prévu actuellement.
Financement/Soutien: Ce travail a été
sponsorisé par la subvention R01 AG20175 du National Institute on Aging
du National Institutes of Health. L'équipe d'intervention GRACE a
été soutenue par le Nina Mason Pulliam Charitable Trust et les
Wishard Health Services d'Indianapolis dans l'Indiana.
Rôle des sponsors: Les sponsors ont fourni un soutien
financier pour l'étude uniquement. Ils n'ont pas participé au
schéma ni à la conduite de l'étude, au recueil, à
la gestion, à l'analyse ou à l'interprétation des
données; ni à la préparation, revue ou approbation du
manuscrit.
Présentations antérieures: Ces données ont
été partiellement présentées à la
réunion annuelle de l'American Geriatrics Society qui s'est tenue le 13
mai 2005 à Orlando en Floride ; à la réunion annuelle de
la Society of General Internal Medicine du 28 avril 2007 à Toronto en
Ontario ; et à la réunion annuelle de l'American Geriatrics
Society du 3 mai 2007 à Seattle dans l'Etat de Washington.
Autres contributions : Nous remercions le docteur Siu L. Hui, PhD,
membre de l'Indiana University Center for Aging Research, de la faculté
de médecine de l'école de médecine de l'Université
d'Indiana à Indianiapolis et du Regenstrief Institute, Inc,
d'Indianapolis, pour son aide dans l'élaboration du schéma
original de cette étude et du plan d'analyse statistique. Elle n'a pas
reçu d'autres compensations que celles offertes par ses
activités normales.
Affiliations des auteurs : Indiana University Center for Aging
Research et Department of Medicine, Indiana University School of Medicine,
Indianapolis; Regenstrief Institute Inc, Indianapolis, Indiana; et Department
of Medicine, University of Wisconsin Medical School, Madison.
BIBLIOGRAPHIE
 |  |
1. Callahan CM, Stump TE, Stroupe KT, et al. Cost of health care for a
community of older adults in an urban academic healthcare system. J
Am Geriatr Soc.1998; 46(11):1371
-1377.
PUBMED
2. A Data Book: Healthcare Spending and the Medicare
Program, June 2005. Washington, DC: Med-PAC; 2005:12
-20.3. Jencks SF, Cuerdon T, Burwen DR, et al. Quality of medical care
delivered to Medicare beneficiaries: a profile at state and national levels.
JAMA.2000; 284(13):1670
-1676.
FREE FULL TEXT
4. Asch SM, Sloss EM, Hogan C, et al. Measuring underuse of necessary
care among elderly Medicare beneficiaries using inpatient and outpatient
claims. JAMA.2000; 284(18):2325
-2333.
FREE FULL TEXT
5. Wenger NS, Solomon DS, Roth CP, et al. The quality of medical care
provided to vulnerable community-dwelling older patients. Ann
Intern Med.2003; 139(9):740
-747.
FREE FULL TEXT
6. Boult C, Boult L, Pacala JT. Systems of care for older populations
of the future. J Am Geriatr Soc.1998; 46(4):499
-505.
PUBMED
7. Reuben DB. Organizational interventions to improve health outcomes
of older persons. Med Care.2002; 40(5):416
-428.
PUBMED
8. Wolff JL, Boult C. Moving beyond round pegs and square holes:
restructuring Medicare to improve chronic care. Ann Intern
Med.2005; 143(6):439
-445.
FREE FULL TEXT
9. Landefeld CS, Palmer RM, Kresevic DM, et al. A randomized trial of
care in a hospital medical unit especially designed to improve the functional
outcomes of acutely ill older patients. N Engl J Med.1995; 332(20):1338
-1344.
PUBMED
10. Counsell SR, Holder CM, Liebenauer LL, et al. Effects of a
multicomponent intervention on functional outcomes and process of care in
hospitalized older patients: a randomized controlled trial of Acute Care for
Elders (ACE) in a community hospital. J Am Geriatr
Soc.2000; 48(12):1572
-1581.
PUBMED
11. Covinsky KE, King JT, Quinn LM, et al. Do acute care for elders
units increase hospital costs? a cost analysis using the hospital perspective.
J Am Geriatr Soc.1997; 45(6):729
-734.
PUBMED
12. Palmer RM, Counsell SR, Landefeld CS. Acute Care for Elders (ACE)
units: practical considerations for optimizing health outcomes. Dis
Manage Health Outcomes.2003; 11(8):507
-517.
13. Counsell SR, Callahan CM, Buttar AB, Clark DO, Frank KI. Geriatric
resources for assessment and care of elders (GRACE): a new model of primary
care for low-income seniors. J Am Geriatr Soc.2006; 54(7):1136
-1141.
PUBMED
14. Eng C, Pedulla J, Eleazer GP, McCann R, Fox N. Program of
All-Inclusive Care for the Elderly (PACE): an innovative model of integrated
geriatric care and financing. J Am Geriatr Soc.1997; 45(2):223
-232.
PUBMED
15. Bernabei R, Landi F, Gambassi G, et al. Randomised trial of impact
of model of integrated care and case management for older people living in
community. BMJ.1998; 316(7141):1348
-1351.
FREE FULL TEXT
16. Hughes SL, Weaver FM, Giobbie-Hurder A, et al. Effectiveness of
team-managed home-based primary care: a randomized multicenter trial.
JAMA.2000; 284(22):2877
-2885.
FREE FULL TEXT
17. Kane RL, Homyak P, Bershadsky B, Flood S, Zhang H. Patterns of
utilization for the Minnesota Senior Health Options program. J Am
Geriatr Soc.2004; 52(12):2039
-2044.
PUBMED
18. Kane RL, Homyak P, Bershadsky B, Flood S. The effects of a variant
of the Program for All-inclusive Care of the Elderly on hospital utilization
and outcomes. J Am Geriatr Soc.2006; 54(2):276
-283.
PUBMED
19. Gravelle H, Dusheiko M, Sheaff R, et al. Impact of case management
(Evercare) on frail elderly patients: controlled before and after analysis of
quantitative outcome data [published online ahead of print November 15, 2006].
BMJ.2007; 334(7583):31
doi:10.1136/bmj.39020.413310.55
.
FREE FULL TEXT
20. Pfeiffer E. A short portable mental status questionnaire for the
assessment of organic brain deficit in elderly patients. J Am
Geriatr Soc.1975; 23(10):433
-441.
PUBMED
21. User Manual FORTRAN Subroutines for Statistical
Analysis. Houston, Tex: IMSL Inc; 2006.22. Kroenke K, Spitzer RL, Williams JB. The PHQ-9: validity of a brief
depression severity measure. J Gen Intern Med.2001; 16(9):606
-613.
PUBMED
23. Wenger NS, Shekelle PG. Assessing care of vulnerable elders: ACOVE
project overview. Ann Intern Med.2001; 135(8 pt 2):642
-646.
FREE FULL TEXT
24. Shekelle PG, MacLean CH, Morton SC, Wenger NS. Assessing care of
vulnerable elders: methods for developing quality indicators. Ann
Intern Med. 2001;135(8
pt 2): 647-652.
FREE FULL TEXT
25. Shekelle PG, MacLean CH, Morton SC, Wenger NS; ACOVE Investigators.
ACOVE quality indicators. Ann Intern Med.2001; 135(8 pt 2):653
-667.
FREE FULL TEXT
26. Higashi T, Shekelle PG, Adams JL, et al. Quality of care is
associated with survival in vulnerable older patients. Ann Intern
Med.2005; 143(4):274
-281.
FREE FULL TEXT
27. Ware JE, Sherbourne CD. The MOS 36-Item Short-Form Health Survey.
Med Care.1992; 30(6):473
-481.
PUBMED
28. Ware JE, Kosinski M, Keller SD. SF-36 Physical and
Mental Health Summary Scales: A User's Manual. Boston, MA: The
Health Institute, New England Medical Center; 1994.29. Ware JE, Bayliss MS, Rogers WH, Kosinski M, Tarlow AR. Differences
in 4-year health outcomes for elderly and poor, chronically ill patients
treated in HMO and fee-for-service systems: results from the Medical Outcomes
Study. JAMA.1996; 276(13):1039
-1047.
FREE FULL TEXT
30. Hauser RM, Willis RJ. Survey design and methodology in the Health
and Retirement Study and the Wisconsin Longitudinal Study. In: Waite L, ed.
Aging, Health, and Public Policy: Demographic and Economic
Perspectives. New York, NY: Population Council;2005
: 208-235.31. Reuben DB, Frank JC, Hirsch SH, McGuigan KA, Maly RC. A randomized
clinical trial of outpatient comprehensive geriatric assessment coupled with
an intervention to increase adherence to recommendations. J Am
Geriatr Soc.1999; 47(3):269
-276.
PUBMED
32. Pacala JT, Boult C, Boult L. Predictive validity of a questionnaire
that identifies older persons at risk for hospital admission. J Am
Geriatr Soc.1995; 43(4):374
-377.
PUBMED
33. Vojta CL, Vojta DD, TenHave TR, Amaya M, Lavizzo-Mourey R, Asch DA.
Risk screening in a Medicare/Medicaid population: administrative data versus
self report. J Gen Intern Med.2001; 16(8):525
-530.
PUBMED
34. Streiner D, Geddes J. Intention to treat analysis in clinical
trials when there are missing data. Evid Based Ment
Health.2001; 4(3):70
-71.
FREE FULL TEXT
35. Singer SD. Using SAS PROC MIXED to fit multilevel models,
hierarchical models, and individual growth models. J Educat Behav
Stat.1998; 23(4):323
-355.
36. Horton NJ, Lipsitz SR. Multiple imputation in practice: comparison
of software packages for regression models with missing variables.
Am Statistician.2001; 55(3):244
-254.
37. Allen KR, Hazelett SE, Palmer RM, et al. Developing a stroke unit
using the acute care for elders intervention and model of care. J
Am Geriatr Soc.2003; 51(11):1660
-1667.
PUBMED
38. Stuck AE, Aronow HU, Steiner A, et al. A trial of annual in-home
comprehensive geriatric assessments for elderly people living in the
community. N Engl J Med.1995; 333(18):1184
-1189.
PUBMED
39. Stuck AE, Egger M, Hammer A, Minder CE, Beck JC. Home visits to
prevent nursing home admission and functional decline in elderly people:
systematic review and meta-regression analysis. JAMA.2002; 287(8):1022
-1028.
FREE FULL TEXT
40. Cohen HJ, Feussner JR, Weinberger M, et al. A controlled trial of
inpatient and outpatient geriatric evaluation and management. N
Engl J Med.2002; 346(12):905
-912.
PUBMED
41. Samsa G, Edelman D, Rothman ML, et al. Determining clinically
important differences in health status measures.
Pharmacoeconomics.1999; 15(2):141
-155.
PUBMED
42. Hays RD, Woolley JM. The concept of clinically meaningful
difference in health-related quality-of-life research: how meaningful is it?
Pharmacoeconomics.2000; 18(5):419
-423.
PUBMED
43. Gill TM, Baker DI, Gottschalk M, Peduzzi PN, Allore H, Byers A. A
program to prevent functional decline in physically frail, elderly persons who
live at home. N Engl J Med.2002; 347(14):1068
-1074.
PUBMED
44. Boult C, Boult LB, Morishita L, Dowd B, Kane RL, Urdangarin CF. A
randomized clinical trial of outpatient geriatric evaluation and management.
J Am Geriatr Soc.2001; 49(4):351
-359.
PUBMED
45. Rubenstein LZ, Alessi CA, Josephson KR, Hoyl MT, Harker JO,
Pietruszka FM. A randomized trial of screening, case finding, and referral
system for older veterans in primary care. J Am Geriatr
Soc.2007; 55(2):166
-174.
PUBMED
46. Leveille SG, Wagner EH, Davis C, et al. Preventing disability and
managing chronic illness in frail older adults: a randomized trial of a
community-based partnership with primary care. J Am Geriatr
Soc.1998; 46(10):1191
-1198.
PUBMED
47. Sommers LS, Marton KI, Babaccia JC, Randolph J. Physician, nurse,
and social worker collaboration in primary care for chronically ill seniors.
Arch Intern Med.2000; 160(12):1825
-1833.
FREE FULL TEXT
48. Wieland D, Lamb VL, Sutton SR, et al. Hospitalization in the
Program of All-Inclusive Care for the Elderly (PACE): rates, concomitants, and
predictors. J Am Geriatr Soc.2000; 48(11):1373
-1380.
PUBMED
49. Burton LC, Weiner JP, Stevens GD, Kasper J. Health outcomes and
Medicaid costs for frail older individuals: a case study of a MCO versus
fee-for-service care. J Am Geriatr Soc.2002; 50(2):382
-388.
PUBMED
50. Ferrucci L, Guralnik JM, Studenski S, et al. Designing randomized,
controlled trials aimed at preventing or delaying functional decline and
disability in frail, older persons: a consensus report.
JAGS. 2004;52:625
-634.
51. Hsu JC. Multiple Comparisons: Theory and
Methods. Columbus, OH: Chapman & Hall/CRC;1996
.52. Unützer J, Katon W, Callahan CM, et al. Collaborative care
management of late-life depression in the primary care setting: a randomized
controlled trial. JAMA.2002; 288(22):2836
-2845.
FREE FULL TEXT
53. Callahan CM, Boustani MA, Unverzagt FW, et al. Effectiveness of
collaborative care for older adults with Alzheimer disease in primary care: a
randomized controlled trial. JAMA.2006; 295(18):2148
-2157.
FREE FULL TEXT
54. Cigolle CT, Langa KM, Kabeto MU, Tian Z, Blaum CS. Geriatric
conditions and disability: the Health and Retirement Study. Ann
Intern Med.2007; 147(3):156
-164.
FREE FULL TEXT
55. Goroll AH, Berenson RA, Schoenbaum SC, Gardner LB. Fundamental
reform of payment for adult primary care: comprehensive payment for
comprehensive care. J Gen Intern Med.2007; 22(3):410
-415.
PUBMED
56. American College of Physicians. The Advanced Medical
Home: A Patient-Centered. Philadelphia,
PA:Physician-GuidedModelofHealthCare;2006:1
-22.
ARTICLE EN RAPPORT
Cette semaine dans le JAMA
JAMA. 2007;298:2587.
Texte Complet
|