 |
 |

Effet d'un vaccin 16/18 L1 à base de particules virales du Papillomavirus humain chez des jeunes femmes ayant une infection préexistanteUn essai randomisé
Allan Hildesheim, PhD;
Rolando Herrero, MD, PhD;
Sholom Wacholder, PhD;
Ana C. Rodriguez, MD;
Diane Solomon, MD;
M. Concepcion Bratti, MD;
John T. Schiller, PhD;
Paula Gonzalez, MD;
Gary Dubin, MD;
Carolina Porras, MQC;
Silvia E. Jimenez, MBA;
Douglas R. Lowy, MD; for the Costa Rican HPV Vaccine Trial Group
RÉSUMÉ
 |  |
Contexte Les vaccins à base de particules virales du
papillomavirus humain (HPV) ont été conçus pour
prévenir l'infection par le HPV infection et le développement de
lésions précancéreuses et de cancers cervicaux. Les
femmes ayant des infections liées à des oncogènes de HPV
pourraient envisager cette vaccination à but thérapeutique.
Objectif Déterminer si la vaccination contre les types 16 et
18 du HPV augmente le taux de clairance virale chez des femmes
déjà infectées par HPV.
Schéma, et environnement Essai de phase III, masqué,
randomisé, ayant pour base une communauté, mené dans deux
provinces du Costa Rica.
Participants Au total, 2189 femmes, âgées de 18
à 25 ans, qui ont été recrutées entre juin 2004 et
décembre 2005. Les participantes étaient positives pour l'ADN
HPV à l'inclusion, avaient au moins 6 mois de suivi, et un suivi des
résultats de l'ADN HVP.
Traitement Les participantes étaient randomisées pour
recevoir sur 6 mois trois doses d'un vaccin candidat bivalent AS04 à
base de particules virales de HPV-16/18 L1 (n=1088) ou un vaccin
contrôle contre l'hépatite A (n=1101).
Principaux critères de jugement La présence d'ADN HPV
a été déterminée dans des échantillons
cervicaux par un test d'hybridation moléculaire utilisant des sondes
chimioluminescentes HPV ARN et par une PCR (réaction en chaîne
à la polymérase) utilisant des déclencheurs de type SPF10
et par un système de détection avec un test type ligne analyse
de sonde avant la vaccination et par PCR après la vaccination. Nous
avons comparé les taux de clairance virale spécifique du type en
utilisant des méthodes d'équations
généralisées d'estimation à la consultation du
6ème mois (après deux doses) et à la consultation du
12ème mois (après 3 doses) dans les deux groupes
d'études.
Résultats Il n'y a pas eu de preuve d'une augmentation de la
clairance virale à 6 et 12 mois dans le groupe recevant le vaccin HPV
par rapport au groupe témoin. Les taux de clairance pour les infections
à HPV-16/18 à 6 mois étaient de 33.4% (82/248) dans le
groupe vaccin HPV et de 31.6% (95/298) dans le groupe témoin
(efficacité du vaccin pour la clairance virale, 2.5%; intervalle de
confiance à 95%, -9.8% à 13.5%). Les taux de clairance du
papillomavirus humain 16/18 à 12 mois étaient de 48.8% (86/177)
dans le groupe vaccin HPV et de 49.8% (110/220) dans le groupe témoin
(efficacité du vaccin pour la clairance virale, -2.0%; intervalle de
confiance à 95%, -24.3% à 16.3%). Il n'y a pas eu de preuve d'un
effet thérapeutique pour une des autres catégories
oncogéniques ou non oncogéniques HPV, chez les femmes recevant
toutes les doses de vaccin, chez les femmes ayant des infections simples, ou
chez les femmes stratifiées en fonction des paramètres
d'inclusion suivants: sérologie HPV-16/18, résultats
cytologiques, charge virale ADN HPV, délai depuis le début des
rapports sexuels, infection par Chlamydia trachomatis ou Neisseria
gonorrhoeae, utilisation d'un contraceptif hormonal, ou tabagisme.
Conclusion Chez des femmes positives pour l'ADN HPV, une vaccination
HPV-16/18 n'accélère pas la clairance du virus et ne doit pas
être utilisée pour traiter des infections prévalentes.
Trial Registration
clinicaltrials.gov
Identifier: NCT00128661
JAMA.
2007;298(7):743-753
De savoir qu'une infection avec un type de papillomavirus humain
(HPV) sur environ 15 types oncogéniques nécessaireau
développement d'un cancer cervical, a permis de mettre en œuvre
des efforts de prévention primaire par l'intermédiaire d'une
vaccination.1
Deux vaccins ayant pour base des particules de protéines virales HPV L1
(VLPs) sont en cours d'évaluation dans des essais cliniques à
large échelle.
2-5
Un vaccin (Gardasil) est un vaccin candidat quadrivalent HPV-16/18 contre le
cancer cervical et contient des VLP de deux types oncogéniques HPV,
HPV-16 et HPV-18, mais aussi des VLP des types HPV 6 et 11, qui ne sont pas
impliquées dans la pathogenèse du cancer cervical, mais sont
associées à des verrues génitales bénignes. Ce
vaccin a été approuvé pour une utilisation chez les
femmes, âgées de 9 à 26 ans aux Etats-Unis et dans
plusieurs autres pays. Le deuxième vaccin (Cervarix) est un vaccin
candidat bivalent HPV-16/18 contre le cancer cervical qui contient des VLP
provenant seulement de deux types oncogéniques HPV, HPV-16 et HPV-18.
Ce vaccin a été approuvé en Australie. Une application
pour être autorisé aux Etats-Unis et dans d'autres pays est en
cours d'examen par la FDA (US Food and Drug Administration) et d'autres
organismes réglementaires.
Il a été démontré que les vaccins basés
sur des particules virales apportent une protection presque complète,
spécifique du type, contre les infections par les types du HPV inclus
dans le vaccin au cours des années initiales suivant la
vaccination.2,3,6
Des preuves préliminaires suggèrent qu'au moins 1 des vaccins
(le vaccin candidat bivalent HPV-16/18 contre le cancer cervical) pourrait
apporter une protection partielle contre les types oncogéniques HPV
phylogénétiquement associés à HPV-16/18 (types HPV
31 et 45).3
La protection contre l'infection initiale apportée par la vaccination
avec les vaccins en cours d'évaluation est considérée
comme étant régulée principalement par des anticorps
neutralisants générés par la
vaccination.7,8
Compatible avec ce concept, des taux élevés d'anticorps sont
observés dans l'organisme et dans le tractus génital
après
vaccination.9-1
Les anticorps ne sont pas typiquement impliqués dans le traitement
des infections intracellulaires après leur installation; toutefois, il
a été démontré également que la vaccination
par HPV induisait des réponses immunitaires cellulaires
traditionnellement impliquées dans l'éradication des
infections.10,12-15
Dirigées contre des cibles antigéniques appropriées, ces
réponses à médiation cellulaire pourraient apporter
certains bénéfices de la vaccination chez des individus
déjà infectés. Compte tenu que l'infection par HPV
dépend du génome viral présent dans les cellules de
l'épithélium basal qui donnent naissance aux cellules des
couches supérieures de et que la protéine L1 est seulement
exprimée dans ces couches cellulaires supérieures, on ne sait
pas si la réponse immune induite par le vaccin dirigée contre L1
aurait un effet curatif potentiel chez les
individus.8
Les études animales ne sont pas en faveur de ces effets
thérapeutiques de la vaccination HPV VLP, mais aucune donnée
publiée chez l'homme n'existe qui réponde directement à
cette
possibilité.16
La plupart des infections à HPV, indépendamment du type,
disparaissent spontanément, typiquement entre 6 mois et 2
ans.17 Le
risque de progression vers une maladie in situ et un cancer invasif est plus
important dans un petit sous-groupe de femmes ayant des infections
persistantes au-delà de cette
période.1
Il est important de savoir si la vaccination apporte un bénéfice
thérapeutique aux femmes infectées dans les pays où le
test de l'ADN HPV a été incorporé dans les programmes de
dépistage du cancer cervical.
18,19
Les femmes dans ces programmes qui sont positives pour HPV peuvent
désirer une vaccination au lieu d'attendre plusieurs mois pour
déterminer si leur infection a disparu ou pour choisir des traitements
basés sur une excision ou une ablation de la zone de transformation
cervicale d'où provient le cancer.
Les protocoles de prise en charge actuels impliquant souvent de tester
à nouveau les femmes positives pour le HPV dans les mois suivant un
résultat initial positif pour le HPV avant que des décisions de
traitement ne soient prises, la compréhension de l'impact de la
vaccination sur la clairance virale au cours des 6 à 12 premiers mois
suivant un premier résultat positif pour le HPV est importante. En cas
d'efficacité pour éliminer des infections établies, il
est raisonnable d'espérer que la vaccination pourrait agir dans ce
délai de temps, compte tenu des taux de séroconversion presque
complète et des taux élevés de réponse immune
observés après 1 ou 2 doses de
vaccin.10-12
Pour répondre directement à la question de savoir si les
femmes positives pour l'ADN HPV doivent être encouragées à
recevoir une vaccination HPV-16/18 dans le cadre d'une stratégie utile
pour induire ou accélérer la clairance de leur infection, nous
avons évalué si les taux de résolution des infections
prévalentes à HPV sont affectées par la vaccination au
sein d'un essai randomisé en cours au sein d'une communauté,
mené au Costa-Rica.
METHODES
Recrutement et éligibilité
Les femmes incluses dans l'évaluation présente sont les
participantes d'un large essai randomisé en cours portent sur 7466
femmes, conçu pour évaluer l'efficacité d'un vaccin
HPV-16/18 VLP formulé avec l'adjuvant AS04 (Cervarix, GlaxoSmithKline
[GSK] Biologicals, Rixensart, Belgium) contre une infection persistante
spécifique des types HPV et associé à des lésions
précancéreuses dues à HPV. Les participantes de notre
essai clinique étaient des femmes, âgées de 18 à 25
ans, résidentes des provinces du Guanacaste et de Puntarenas au
Costa-Rica qui étaient identifiées par un nouveau recensement de
population. Les femmes identifiées par ce recensement étaient
invitées à participer par lettre envoyée à
domicile par les membres de l'étude. Les femmes qui venaient à
une des 7 consultations de l'étude étaient
dépistées pour vérifier leur éligibilité
entre le 28 juin 2004 et le 21 décembre 2005.
Pour être éligibles dans cette étude, les femmes
devaient répondre aux critères suivants au moment de leur
inclusion: âge 18 à 25 ans (inclus), résidence
prévue dans la zone de l'étude pendant 6 mois après leur
inclusion, capacité à parler ou comprendre l'espagnol, une bonne
santé générale, déterminée par leurs
antécédents et leur examen clinique et la volonté de
fournir un consentement éclairé écrit.
Les critères spécifiques d'exclusion à l'inclusion
comprenaient les états d'immunodéficience chronique
nécessitant un traitement; les antécédents de
réaction allergique à tout vaccin ou tout état
significatif allergique, une allergie suspectée ou des réactions
aux composés du vaccin ou au latex; des antécédents de
vaccination contre le virus de l'hépatite A ou d'infection par le virus
de l'hépatite A; des antécédents d'administration
récente (<6 mois) et à long terme d'immunosuppresseurs ou
d'immuno-modulateurs ; et le refus d'utiliser une méthode efficace de
contraception pendant la période couvrant la phase de vaccination de
l'essai (chez les personnes sexuellement actives). L'inclusion de femmes
enceintes était remise jusqu'au moins le 3ème mois suivant
l'accouchement et en l'absence d'allaitement au sein.
Aucun dépistage de l'ADN HPV ou des anticorps n'était
réalisé avant l'inclusion/vaccination. L'essai a
été revu et approuvé par les comités
d'éthique du National Cancer Institute aux Etats-Unis et par le
INCIENSA (Instituto Costarriciense de Investigacion y Ensenanza en Nutricion y
Salud) au Costa-Rica.
Données et recueil des échantillons avant la randomisation/vaccination
Un questionnaire sur les facteurs de risque était donné
à toutes les participantes éligibles qui désiraient
participer. Un examen gynécologique était effectué chez
toutes les femmes sexuellement actives, au cours duquel les cellules
exfoliées étaient recueillies dans un médium liquide
(Cytyc Corp, Marlborough, Massachusetts) pour une évaluation
cytologique Thinprep (Cytec Corp) et pour une recherche d'ADN HPV, de
Chlamydia trachomatis, et de Neisseria gonorrhoeae. Des échantillons
sanguins étaient aussi recueillis chez tous les participants avant la
randomisation et la vaccination ; des échantillons sériques
étaient aussi recueillis à partir de ces échantillons
pour recherche d'anticorps HPV.
Randomisation/Vaccination
Les femmes de notre essai étaient randomisées en aveugle dans
le centre pour recevoir soit le vaccin HPV-16/18 VLP avec l'adjuvant AS04 ou
un vaccin contre le virus de l'hépatite A comprenant un antigène
viral inactivé par alun (Havrix, GSK Biologicals). Les vaccins de
l'étude et des témoins étaient délivrés de
façon randomisée par des nombres d'identification au moment de
l'étiquetage chez le fabricant. Le personnel de l'étude dans le
centre d'étude au Costa-Rica randomisait les participantes en assignant
chaque participante éligible au nombre d'identification suivant du
vaccin disponible de manière séquentielle. Le protocole
demandait l'administration d'une dose de vaccin à chacune des trois
consultations de l'étude: à l'inclusion, un mois après la
dose initiale (extrêmes permis, 21-120 jours), et 6 mois après la
dose initiale (extrêmes permis, 121-300 jours). A la consultation du
6ème mois, il était conseillé à toutes les femmes
sexuellement actives de recueillir ellesmêmes un échantillon
cervico-vaginal à l'aide d'un écouvillon en Dacron. Les cellules
exfoliées recueillies étaient stockées dans une solution
Preservcyt et utilisées pour un test ADN HPV. A la suite de ce recueil,
les femmes qui, à l'entrée de l'étude, avaient des signes
soit de cellules squameuses atypiques de signification incertaine positives
pour HPV au test d'hybridation moléculaire utilisant des sondes ARN HPV
chimioluminescentes (the Hybrid Capture 2 [HC2] test; Digene Corp, Silver
Spring, Maryland) soit des lésions intra-épithéliales
squameuses de faible grade, avaient un examen gynécologique. Au moment
de cet examen, un échantillon cervical était aussi recueilli par
un médecin et conservé dans une solution Preservcyt.
Suivi
A la suite de la phase initiale de vaccination, toutes les participantes
devaient retourner à l'une des consultations de l'étude environ
un an après l'inclusion (visite du 12ème mois). Au moment de
cette consultation annuelle de dépistage, un examen
gynécologique était effectué (chez les femmes
sexuellement actives) et les cellules exfoliées étaient
recueillies par un médecin pour évaluation cytologique et un
test d'AND HPV de manière similaire à celle décrite pour
l'inclusion. Un suivi supplémentaire des participantes au-delà
de la période de 12 mois est en cours.
Suivi de la tolérance
Les participantes restaient à la consultation pendant 30 à 60
minutes après chaque vaccination. La
réactogénicité et les événements
indésirables étaient enregistrés auprès de toutes
les participantes au cours de la période et au cours de la semaine
suivant chaque vaccination par des visites à domicile pour un
échantillon randomisé d'environ 10% des participantes. Les
événements indésirables et des informations sur les
grossesses étaient aussi activement recueillis chez toutes les
participantes à chacune des consultations de suivi. De plus, un
numéro de téléphone gratuit, continuellement disponible
grâce au personnel clinique, pouvait être appelé et les
participantes pouvaient appeler ce numéro entre les consultations si un
problème médical se développait.
Un comité de surveillance des données et de la
tolérance (DSMB) mis sur pied par le National Cancer Institute pour
surveiller l'essai se réunissait régulièrement pour
évaluer les données de tolérance en session fermée
(date de la réunion la plus récente: 19 juin 2007). Le DSMB a
recommandé la continuation de l'essai. Le statisticien de
l'étude (S.W.) participait aux revues de ses sessions fermées
sur les tableaux résumés des événements
indésirables par groupe, mais n'était pas impliqué dans
la formulation des recommandations finales du DSMB. L'essai en cours
étant encore en aveugle, les autres investigateurs et le personnel du
site n'ont eu aucun accès aux données de tolérance par
groupe de traitement; en conséquence, aucune donnée de
tolérance n'est présentée ici. Les données de
tolérance et les principaux résultats d'efficacité
prophylactique seront rapportés lorsque l'analyse finale de l'essai
principal sera commencée.
Test ADN HPV
Un test sur l'ADN du papillomavirus humain était effectué sur
les échantillons de l'inclusion (pré-vaccination) à
l'aide d'un aliquot de 2 ml de cellules exfoliées conservées
dans une solution Preservcyt. Le test était pratiqué à
l'aide d'une sonde B (conçue pour détecter 13 types
oncogéniques HPV incluant les types 16, 18, 31, 33, 35, 39, 45, 51, 52,
56, 58, 59, et 68) selon les instructions du fabricants dans un laboratoire
situé à l'Université du Costa Rica à San
José.20
Un test ADN HPV basé sur une PCR à large spectre était
réalisé par le laboratoire Delft Diagnostics (Delft, Pays-Bas)
à l'aide d'une procédure précédemment
décrite utilisant une amplification à l'aide de
déclencheurs SPF10 et par une détection immuno-enzymatique de
l'ADN des amplimères, avec, en cas de positivité, un typage
utilisant un test type ligne analyse de sonde (LiPA) et un système de
détection line blot (Inno-LiPA HPV genotyping assay SPF10 system,
version 1, Labo Bio-medical Products, Rijswijk, Pays-Bas).21-23 Le test LiPA
détecte 25 génotypes HPV (6, 11, 16, 18, 31, 33, 34, 35, 39, 40,
42, 43, 44, 45, 51, 52, 53, 54, 56, 58, 59, 66, 68/73, 70, et 74). Ce test
était réalisé sur un aliquot de 0.5 ml de solution
Preservcyt prélevée d'un échantillon cytologique avant
les préparations de lamelles pour diminuer le risque
d'altération. De plus, en utilisant l'ADN extraite du même
aliquot, et pour s'assurer que les infections HPV-16 et HPV-18
n'étaient pas manquées, tous les échantillons qui
étaient positifs pour l'ADN HPV au test immuno-enzymatique SPF10 ADN,
mais négatifs pour HPV-16 ou HPV-18 au LiPA, étaient
testés pour l'ADN HPV-16 et HPV-18 à l'aide de
déclencheurs spécifiques du type, comme
précédemment
décrit.23,24
Les échantillons à l'inclusion (pré-vaccination) et
les échantillons recueillis aux consultations du 6ème et
12ème mois étaient testés par une méthode de PCR.
Pour les consultations à l'inclusion et au 12 mois, les
échantillons cervicaux recueillis au cours de l'examen
gynécologique étaient utilisés. Pour la consultation du
6ème mois, les échantillons cervico-vaginaux recueillis par les
femmes étaient utilisés. De plus, pour le sous-groupe de femmes
qui avaient eu un examen gynécologique au moment de la consultation du
6ème mois, les échantillons cervicaux recueillis au cours de
l'examen gynécologiques étaient utilisés pour le test
d'ADN HPV par PCR.
Chez 672 femmes ayant recueilli leurs échantillons et en ayant
recueillis par le médecin à la consultation de 6 mois, un
degré important de concordance a été observé pour
les résultats HPV pour ces deux types d'échantillons. L'accord
et les valeurs K pour la détection du HPV entre les
échantillons recueillis par les patientes et ceux par les
médecins ont été de 96.0% and K =0.86 (McNemar
P=0.56, sans donner d'indication directionnelle) pour HPV-16 et 97.6% et
K =0.81 (McNemar P<0.99) pour HPV-18. L'accord global (tous types) a
été de 89.4% avec K =0.59 (McNemar P=0.19). Compte tenu
de ce haut niveau d'accord, les résultats des tests HPV à l'aide
des échantillons auto-recueillis ont été utilisés
pour définir le statut HPV à la consultation du 6ème
mois.
Test de recherche d'anticorps HPV-16/18
Un test d'immuno-absorption immuno-enzymatique a été utilise
pour évaluer les échantillons sériques recueillis chez
les participantes à l'inclusion (pré-vaccination) pour chercher
les anticorps dirigés contre HPV-16 et HPV-18, à l'aide de
méthodes précédemment
décrites.10
Le test a été effectué à GSK Biologicals à
Rixensart, Belgique.
Test de recherche de l'ADN du
Chlamydia trachomatis et Neisseria gonorrhoeae.
La presence d'une infection par C trachomatis et N gonorrhoeae était
déterminée par un test cherchant la présence d'ADN de ces
agents pathogènes dans un aliquot de 2 ml de cellules exfoliées
recueillies à l'inclusion (pré-vaccination) et conservées
dans une solution Preservcyt. La méthode HC2 a été
utilisée selon les instructions du
fabricant.25
Un test a été réalisé dans un laboratoire
situé à l'Université du Costa Rica.
Analyse statistique
Les analyses de données étaient dirigées par les
co-investigateurs principaux de l'étude (A.H. et R.H.) et le
statisticien de l'essai (S.W.). Les analyses étaient effectuées
par un personnel programmateur au centre de prise en charge des données
de l'essai (Information Management Services Inc, Silver Spring, Maryland) sous
contrat direct et supervision du National Cancer Institute et traitées
selon les procédures opérationnelles standards qui s'assurent de
la conservation de la procédure en aveugle et de
l'intégrité globale de l'essai. Les investigateurs, le personnel
de l'étude et les participantes ne connaissaient pas l'assignation des
participantes dans les groupes de vaccin.
Des comparaisons entre les groupes d'étude en fonction des
caractéristiques générales ont été faites
à l'aide d'un test du chi-2 pour les variables catégorielles et
par le test de Wilcoxon pour les variables continues. Chez les femmes
infectées, 42.6% avaient plus d'un type de virus HPV à
l'inclusion. Nous avons choisi d'utiliser une infection plutôt qu'une
femme comme unité de l'analyse en raison de notre intérêt
pour la clairance des types individuels HPV.
Nous avons évalué les catégories suivantes HPV :
HPV-16; HPV-18; HPV-16/18 (HPV-16 et/ou HPV-18); types HPV des espèces
alpha-9, en excluant HPV-16 (types HPV 31, 33, 35, 52, et 58); types HPV des
espèces alpha-7, en excluant HPV-18 (types HPV 39, 45, 59, et 70;
HPV-68 n'a pas été envisagé dans cette catégorie
car le LiPA ne peut différencier HPV-68 de HPV-73); les types
oncogéniques HPV autres que ceux des espèces alpha-7 et alpha-9
(types HPV 51, 56, 66, et 68/73); et types non oncogéniques HPV (types
HPV 6, 11, 34, 40, 42, 43, 44, 53, 54, et 74). Par ailleurs, nous avons
évalué la positivité HPV par un test HC2 à
l'inclusion, car l'évaluation de ce groupe est pertinente d'un point de
vue de prise en charge clinique.
Le pourcentage de clairance a été évalué
indépendamment à la consultation du 6ème mois
(après deux doses de vaccin) et à la consultation du
12ème mois (après 3 doses de vaccin). La clairance virale d'un
type spécifique du HPV était définie comme
l'impossibilité de détecter à la consultation du
6ème et du 12ème mois un type HPV qui était
présent avant la vaccination. Pour l'analyse de la clairance virale
chez les femmes qui étaient positives HC2 à l'inclusion, la
clairance virale était définie par l'absence aux consultations
du 6ème et 12ème mois des types HPV détectés
à l'inclusion par un test spécifique de type par PCR. Celles qui
étaient positives à l'inclusion ou lors du suivi par analyse HC2
mais négatives pour tous les types spécifiques testés
(HC2-positive/SPF10-positive/LiPA négative) étaient
considérées comme positives pour un type inconnu.
Les femmes qui étaient positives pour un type inconnu à
l'inclusion et au cours du suivi étaient considérées
comme ayant une infection persistante (n=13 ou 0.5% de toutes les infections
à 6 mois; n=13 ou 0.7% de toutes les infections à 12 mois). Les
femmes positives à l'inclusion pour un type inconnu qui étaient
positives pour un HPV connu à la visite de suivi étaient
considérées comme ayant éliminé leur infection
initiale et comme ayant acquis une nouvelle infection (n=46 ou 1.7% de toutes
les infections à 6 mois; n=31 ou 1.5% de toutes les infections à
12 mois). Identiquement, les femmes positives à l'inclusion pour un
type connu qui étaient positives pour un type inconnu à la
consultation de suivi, étaient considérées comme ayant
éliminé leur infection initiale et acquis une nouvelle infection
(n=89 ou 3.3% de toutes les infections à 6 mois; n=98 ou 4.9% de toutes
les infections à 12 mois).
L'efficacité du vaccin pour éliminer le virus (clairance
virale) (VEVC), une mesure du pourcentage de réduction (ou
d'augmentation) des taux d'infections observées lorsque le groupe
vaccin HPV est comparé au groupe contrôle, était
définie par (Pr [persistance virale dans le groupe témoin]-Pr
[persistance virale dans le groupe vaccin HPV])/Pr (persistance virale dans le
groupe témoin)=1-(Pr [persistance virale dans le groupe vaccin HPV]/Pr
[persistance virale dans le groupe témoin])=1-RR, où Pr
représente la probabilité de persistance à un moment
d'intérêt (6 ou 12 mois) et RR est le rapport de
probabilité (risque) de persistance dans les deux groupes. Des
intervalles de confiance (IC95%) à 95% autour des estimations VEVC ont
été informatisés à partir des IC pour le RR.
Une méthode généralisée des équations
d'estimation a été utilisée pour prendre en compte
l'absence possible d'indépendance entre les clairances dans l'analyse
de plus d'une infection chez la même
patiente.26
Les estimations du pourcentage d'infections qui ont disparu de l'analyse
généralisée des équations d'estimation peuvent
donc être légèrement différentes des pourcentages
crus. Nous présentons VEVC contre la persistance de plusieurs
catégories de HPV aux consultations de 6 mois et 12 mois de même
qu'une analyse restreinte aux femmes qui avaient reçu toutes les doses
de vaccin et celles ayant des signes d'un type unique HPV à
l'inclusion. D'autres analyses ont été effectuées pour
évaluer VEVC stratifiées en fonction des paramètres
d'intérêt suivants à l'inclusion : anticorps HPV-16/18
(positive pour l'un ou l'autre vs négatifs pour les deux), observations
cytologiques (cellules squameuses normales vs atypiques de signification
incertaine), charge virale HC2 (valeurs relatives unité, 0-<2.0,
2.0-<50, et 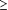 50), mois depuis le début de l'activité
sexuelle (0-36 mois, 37-72 mois, et 50), mois depuis le début de l'activité
sexuelle (0-36 mois, 37-72 mois, et 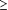 73 mois), utilisation de
contraceptifs oraux ou injectables (utilisation actuelle vs utilisation non
actuelle), tabagisme (fumeurs actuels vs fumeurs non actuels), et observations
chlamydia/gonorrhée (positives pour l'un ou l'autre ou négatives
pour les deux). 73 mois), utilisation de
contraceptifs oraux ou injectables (utilisation actuelle vs utilisation non
actuelle), tabagisme (fumeurs actuels vs fumeurs non actuels), et observations
chlamydia/gonorrhée (positives pour l'un ou l'autre ou négatives
pour les deux).
RESULTATS
Population de l'étude
Au total, 7466 femmes ont été incluses et randomisées
(FIGURE). Pour
l'évaluation actuelle, nous avons exclu 4 femmes qui avaient
reçu par erreur les deux types de vaccin. Chez les 7462 femmes
restantes, 3726 ont été randomisées dans le groupe vaccin
HPV et 3736 dans le groupe témoin. Au total, 1594 femmes (775 dans dans
le groupe vaccin HPV et 819 dans le groupe témoin) n'ont pas
été incluses dans l'évaluation actuelle car elles
n'avaient pas eu de relation sexuelles à l'inclusion (n = 1591) ou
parce qu'un examen gynécologique ne pouvait être effectué
pour d'autres raisons (n=3). Cent-dix femmes de plus (60 dans le groupe vaccin
HPV et 50 dans le groupe témoin) ont été exclus en raison
de preuves de lésions intra-épithéliales squameuses de
haut grade ou d'atteinte plus sévère à l'inclusion, ayant
entraîné leur envoi à une unité de colposcopie pour
évaluation et possible traitement. Ce groupe a été exclu
pour éviter tout effet d'une suppression de traitement sur la
persistance virale.
|
|

|
|
Figure.. Distribution des participantes
HPV correspond à papillomavirus humain ; PCR, réaction en
chaîne à la polymérase.
aRésultats non disponibles au moment de l'arrêt des
données (arrêt des données : 29 mars 2007, pour la base de
données cliniques ; 26 juin 2006, pour la base de données sur le
questionnaire des facteurs de risque; 25 avril 2007, pour la base de
données HPV PCR; et 17 juillet 2006, pour la base de données
sérologique HPV-16/18).
bL'analyse de clairance des infections Hybrid Capture
2-positives détectées à l'inclusion étaient
basées sur 666 femmes dans le groupe vaccin HPV et sur 663 femmes dans
le groupe témoin, ainsi qu'il est décrit dans la section
"Méthodes" du texte.
cInclut 134 femmes (56 dans le groupe vaccin HPV et 78 dans le
groupe témoin) qui n'avaient pas de résultats HPV PCR
disponibles à la consultation des 6 mois.
|
|
|
Parmi les 5758 participantes restantes, 2376 (41.3%; 1194 dans le groupe
vaccin HPV et 1182 dans le groupe témoin) étaient positives pour
l'ADN HPV à l'inclusion dans l'étude avec le SPF10/LiPA ou par
PCR avec déclencheur spécifique du type HPV-16/18. Un typage
individuel n'a pu être obtenu chez 455 autres femmes (7.9%)
(SPF10-positives/LiPA-négatives et négatives à la PCR
avec déclencheur spécifique du type HPV-16/18. Un typage
individuel n'a pu être obtenu chez 455 autres femmes (7.9%)
(SPF10-positives/LiPA-négatives et négatives à la PCR
avec déclencheur spécifique du type HPV-16/18); ces femmes n'ont
pas été incluses dans les analyses principales car
l'évaluation de la clairance virale nécessite une connaissance
des types spécifiques HPV impliqués. Parmi les 2376 femmes
positives pour HPV à la SPF-10/LiPA lors de l'inclusion, 321 (162 dans
le groupe vaccin HPV et 159 dans le groupe témoin) ont
été exclues des analyses principales, car elles n'avaient les
résultats disponibles de la PCR pour le HPV lors de leur consultation
des 6 mois. Les résultats de la PCR manquaient pour ces 321 femmes en
raison de leur absence aux consultations (n=285) ou d'interruption
d'étude (n=33) ou parce que les résultats de la PCR
n'étaient pas encore disponibles au laboratoire d'analyses (n=3).
Par rapport aux femmes incluses dans l'analyse, les 321 femmes exclues,
tendaient à être légèrement plus jeunes (âge
moyen, 20.6 ans pour celles exclues vs 21.3 ans pour celles incluses ;
P<0.001) mais étaient comparables par rapport au nombre de
partenaires sexuels sur une vie moyenne (P=0.12), à la fréquence
des observations cytologiques anormales à l'inclusion (P=0.64), au
pourcentage d'individus ayant de multiples infections (P=0.16), et à la
distribution des groupes d'analyse HPV (P=0.29). Un taux plus faible
d'orientation pour colposcopie après inclusion a été
observé chez celles exclues de l'analyse (5.9% vs 15.7% chez celles
incluses; P<0.001). Ces 321 femmes étaient comparables par groupe
pour l'âge (P=0.34), le nombre sur une vie de partenaires sexuels
(P=0.54), le pourcentage de participantes orientées vers une
colposcopie au cours de suivi (P=0.25), le pourcentage de patientes ayant de
multiples infections (P=0.70), et la distribution des groupes d'analyse HPV
(P=0.25). Un nombre plus important de de cytologies anormales à
l'inclusion a été observé dans le groupe vaccin HPV
(36.6% vs 25.2%; P=0.03).
Le nombre final de femmes dans les analyses HPV PCR a été de
2055 (1032 dans le groupe vaccin HPV et 1023 dans le groupe témoin ;
P=0.84). Ces femmes avaient au total 3467 infections à l'inclusion
(1730 dans le groupe vaccin HPV et 1737 dans le groupe témoin ;
P=0.91).
Au total, 1671 femmes (825 dans le groupe vaccin HPV et 846 dans le groupe
témoin; P=0.61) avaient les résultats de la PCR disponibles
à la consultation du 12ème mois, dont 134 femmes (56 dans le
groupe vaccin HPV et 78 dans le groupe témoin) n'avaient pas de
résultats de la PCR disponibles à la visite du 6ème mois.
Les résultats de la PCR n'étaient pas disponibles chez 705
femmes en raison de consultations manquées (n=456) ou d'interruption de
l'étude (n=65), ou parce que les résultats de la PCR
n'étaient pas revenus du laboratoire d'analyse (n=87), ou parce que la
consultation du 12ème mois n'avait pas été menée
au moment de cette analyse (n=97).
Parmi les 705 femmes exclues, 341 (48.4% vs 0 chez celles incluses dans
l'analyse; P<0.001) avaient des données du 12ème mois
manquantes en raison de leur orientation vers une colposcopie après
leur entrée dans l'étude. En conséquence, les femmes
exclues de cette analyse du 12ème mois différaient de celles
incluses pour certains facteurs comme l'orientation vers une colposcopie,
l'âge moyen (20.9 ans vs 21.4 ans; P<0.001), le nombre moyen sur une
vie de partenaires sexuels (2.9 vs 2.7; P=0.002), la fréquence
d'observations anormales cytologiques à l'inclusion (62.8% vs 16.1%;
P<0.001), et le pourcentage de personnes ayant des infections multiples
à HPV (50.1% vs 40.2% ; P<0.001). Toutefois, ces différences
n'ont pas été différentielle selon les groupes
d'étude; les 705 femmes étaient comparables selon le groupe pour
l'âge (P=0.22), le nombre de partenaires sexuels sur une vie (P=0.77),
les observations cytologiques anormales à l'inclusion (P=0.93), le
pourcentage de participantes orientées vers une colposcopie au cours du
suivi (P=0.50), le pourcentage de patientes ayant de multiples infections
(P=0.24), et la distribution des groupes d'analyse HPV (P=0.10).
Différentes exclusions ont été appliquées pour
l'analyse basée sur les résultats à l'inclusion du test
HC2, car l'intention de cette analyse spécifique était
d'examiner les effets du vaccin dans un groupe de femmes positives pour HPV
par un test clinique HC2. Chez 5758 femmes ayant eu un examen
gynécologique non orientées vers une colposcopie à
l'inclusion, 3711 (1866 dans le groupe vaccin HPV et 1845 dans le groupe
témoin) ont été exclues car elles étaient
HC2-négatives, 181 (92 dans le groupe vaccin HPV et 89 dans le groupe
témoin) ont été exclues car les résultats du test
HC2 étaient manquants à l'inclusion, et 104 (59 dans le groupe
vaccin HPV et 45 dans le groupe témoin) ont été exclues
car elles étaient positives pour HC2 mais négatives aux
résultats de la PCR.
Au total, 1762 (874 dans le groupe vaccin HPV et 888 dans le groupe
témoin) étaient positives pour HPV ADN à la fois au test
HC2 et par PCR. Le groupe final de cette analyse comprenait 1520 femmes sur
ces 1762 chez lesquelles les résultats des analyses HPV étaient
disponibles à la consultation du 6ème mois (752 dans le groupe
vaccin HPV et 768 dans le groupe témoin; P=0.68). Au total, 1169 de ces
femmes (574 dans le groupe vaccin HPV et 595 dans le groupe témoin;
P=0.54) avaient aussi des résultats HPV PCR disponibles pour la
consultation du 12ème mois, dont 101 femmes (43 dans le groupe vaccin
HPV et 58 dans le groupe témoin) qui n'avaient pas de résultats
HPV PCR disponibles à la consultation du 6ème mois. Les dates
d'arrêt des données pour ces différents composants des
données de l'étude ont été les suivantes: base de
données cliniques, 29 mars 2007; questionnaire sur les facteurs de
risque, 26 juin 2006; base de données HPV PCR, 25 avril 2007; et base
de données sur la sérologie HPV-16/18, 17 juillet 2006.
Les caractéristiques des participantes incluses dans cette analyse
ont été comparées entre les groupes. Les résultats
sont résumés dans le tableau
1. Les 1088 participantes du groupe vaccin HPV et les 1101
participantes du groupe témoin étaient comparables pour
l'âge à l'inclusion, le nombre de partenaires sexuels sur une
vie, les observations cytologiques à l'inclusion, le pourcentage de
participantes orientées vers une colposcopie au cours du suivi, le
pourcentage de patients ayant des infections multiples, et la distribution des
groupes d'analyse HPV. Le nombre de doses reçues et les intervalles
entre l'inclusion et les consultations à 1 mois, 6 mois et 12 mois
étaient aussi comparables parmi les groupes
(Tableau 1).
|
|

|
|
Tableau 1.. Caractéristiques des participantesa
Abréviation: HPV, papillomavirus humain.
aLes données sont exprimées sous la forme de
nombre de (%) participantes sauf indication contraire. Les données
incluent toutes les femmes dans les analyses de 6 et 12 mois, dont les 134
femmes évaluées dans la seule analyse à 12 mois. Une
femme du groupe vaccin HPV avait 26 ans à l'inclusion; 7 femmes (1 du
groupe vaccin HPV et 6 du groupe témoin) avaient des informations
manquantes sur le nombre de partenaires sexuels dans une vie; 8 femmes (4 du
groupe vaccin HPV et 4 du groupe témoin) avaient des résultats
cytologiques manquants.
bL'orientation vers une colposcopie après inclusion dans
l'étude trial était basée sur les preuves de
lésions intra-épithéliales squameuses de faible grade ou
sur la présence cellules squameuses atypiques HPV positives de
signification incertaine à
cl'inclusion et à la visite de 6 mois ou sur des preuves
de lésions intra-épithéliales squameuses de haut grade ou
une maladie plus sévère à la consultation de 6 mois. Le
chiffres dans les groupes d'analyse HPV additionnés donnent plus que le
total du nombre de femmes car certaines femmes avaient des infections
multiples. Les pourcentages étaient calculés pour le niveau
d'infection.
|
|
|
Clairance virale du HPV
Les taux de clairance virale aux consultations du 6ème mois et du
12ème mois et les estimations VEVC pour HPV-16, HPV-18, et HPV-16/18
combinées sont présentés dans le tableau le
TABLEAU 2.
|
|

|
|
Tableau 2.. Clairance virale et efficacité du vaccin pour la clairance virale
dans les groupes d'étude HPV-16 et HPV-18 à 6 mois et 12 mois de
suivi.
Abréviations: IC, intervalle de confiance; HPV, papillomavirus
humain.
aPourcentages calculés à l'aide de méthodes
généralisées d'équations d'estimation et pouvant
donc varier des pourcentages bruts.
bHPV-16/18 est défini par HPV-16 et/ou HPV-18.
cToutes les doses sont définies par 2 doses au
6ème mois et 3 doses au 12ème mois.
|
|
|
A la consultation du 6ème mois, les taux de clairance étaient
de 27.3% vs 27.5% pour HPV-16, 46.1% vs 44.7% pour HPV-18, et 33.4% vs 31.6%
pour HPV-16/18 chez les participantes qui avaient respectivement reçu
les vaccins HPV et le vaccin contrôle. A la consultation du 12ème
mois, les taux de clairance chez les participantes dans le groupe HPV et le
groupe contrôle, étaient respectivement de 43.9% vs 45.9% pour
HPV-16, 59.3% vs 60.7% pour HPV-18, et 48.8% vs 49.8% pour HPV-16/18.
Il n'y a pas eu de preuve que la vaccination HPV ait modifié
significativement les taux de clairance virale; les estimations VEVC allaient
globalement de - 0.2% à 2.5% à la consultation du 6ème
mois et de -3.7% à -2.0% à la consultation du 12ème mois.
Pour les infections HPV-16/18, les estimations VEVC étaient de 2.5% (IC
95%, -9.8% à 13.5%) à la consultation du 6ème mois et de
-2.0% (IC 95%, -24.3% à 16.3%) à la consultation du 12ème
mois. Aucune preuve significative d'un effet thérapeutique du vaccin
n'a été observée dans les analyses restreintes aux femmes
ayant reçu toutes les doses du vaccin ou chez celles ayant la preuve
d'une seule infection HPV à l'inclusion
(Tableau 2). Nous n'avons
observé aucune preuve des effets du vaccin lorsque nous avons
stratifié l'analyse sur les caractéristiques d'inclusion dans
l'étude reflétant l'étendue de la maladie, dont les
résultats des anticorps HPV-16/18, les résultats cytologiques et
la charge virale HPV (TABLEAU
3). De même, aucune preuve des effets du vaccin n'a
été observée dans les analyses stratifiées en
fonction des autres paramètres d'inclusion dans l'étude pouvant
influencer potentiellement les taux de clairance et l'efficacité du
vaccin, dont le temps écoulé depuis le début des rapports
sexuels, l'utilisation d'un contraceptif, le tabagisme et une infection
concomitante à C trachomatis ou N gonorrhoeae
(Tableau 3).
|
|

|
|
Tableau 3.. Clairance virale et efficacité du vaccin sur la clairance virale de
HPV-16/18 par groupe d'étude à 6 mois et 12 mois de suivi
stratifiée par facteurs sélectionnésa
Abréviations : IC, intervalle de confiance; HC2, Test Hybrid Capture
2; HPV, papillomavirus humain.
aHPV-16/18 est défini par HPV-16 et/ou HPV-18.
bLes pourcentages sont calculés à l'aide de
méthodes généralisées d'équations
d'estimations et peuvent donc varier des pourcentages bruts.
|
|
|
Le TABLEAU 4 montre les
résultats des analyses qui ont évalué les taux de
clairance virale et les VEVC pour les catégories HPV autres que HPV-16
et HPV-18. Les taux de clairance virale à la consultation du
6ème mois pour ces autres catégories HPV étaient plus
élevés que pour HPV-16 en particulier, allant de 44.6% à
61.1% dans le groupe témoin; les taux de clairance à la
consultation du 12ème mois allaient de 59.2% à 78.1%. Il n'y a
pas eu de preuve que la vaccination HPV diminuait significativement les taux
de clairance virale (les estimations VEVC allaient de -7.6% à 7.6%
à la consultation du 6ème mois et de -8.7% 12.2% à la
consultation du 12ème mois).
|
|

|
|
Tableau 4.. Clairance virale et efficacité du vaccin sur la clairance virale
pour les autres catégories de HPV par groupe d'étude aux suivis
de 6 et 12 mois.
Abréviations : IC, intervalle de confiance; HC2, Test Hybrid Capture
2; HPV, papillomavirus humain.
aLes pourcentages sont calculés à l'aide de
méthodes généralisées d'équations
d'estimations et peuvent donc varier des pourcentages bruts.
|
|
|
COMMENTAIRES
 |  |
Nous avons évalué l'effet d'une vaccination de type HPV VLP
sur la clairance virale chez les participantes de notre étude
d'efficacité au Costa Rica alors qu'elles étaient porteuses
d'une infection prévalente au moment de la vaccination. L'essai avait
l'avantage d'être effectué au sein de la communauté (les
participantes étaient identifiées par un recensement de la
population) et randomisée. Nos résultats montrent que le taux de
clairance virale sur une période de 12 mois n'est pas influencé
par la vaccination. Globalement, les estimations VEVC obtenues ont
été proches de 0%, et les IC à 95% (ex, -24.3% à
16.3% pour HPV-16/18 à 12 mois) suggèrent que, même si la
vaccination procure un certain bénéfice, il est probablement
faible. Les estimations de puissance post hoc sont de 82%, 98% et 99% pour
évaluer l'hypothèse que l'efficacité du vaccin pour la
clairance de HPV-16/18 à 12 mois est respectivement de 30%, 40%, ou
50%.
Ces observations ont d'importantes implications cliniques. Ainsi, dans les
pays où l'évaluation de l'ADN HPV est incorporé dans le
dépistage du cancer du sein et les efforts de prévention,19 les
femmes adultes ayant un frottis cervical anormal induit par une infection par
le HPV et/ou positives pour un type oncogénique HPV au test HC2 peuvent
avoir un intérêt à recevoir un vaccin HPV pour traiter
leur infection existante. Nos résultats montrent que les praticiens ne
doivent pas encourager l'utilisation des vaccins L1 VLP dans ce but. Bien que
les vaccins VLP HPV aient peu de probabilité de procurer des
bénéfices dans le traitement des infections prévalentes,
les femmes ayant des infections établies peuvent en
bénéficier individuellement dans d'autres indications. Du point
de vue de la population (ou de la santé publique), il n'est toutefois
pas sûr que, chez les femmes infectées par le HPV, le
bénéfice résiduel pour prévenir une infection par
les types HPV du vaccin auxquels les femmes n'ont pas été
exposées, serait suffisant pour rendre une vaccination
nécessaire. Toutefois, les HPV étant des virus communs
très fréquents auxquels les femmes sont typiquement
exposées au cours des mois initiaux ou des années suivant le
début des rapports sexuels,1 la vaccination des femmes après
leur exposition et leur infection (c-à-d., après le pic
d'exposition) apporte probablement moins de bénéfice que la
vaccination des femmes avant leur exposition initiale. Ceci contraste avec les
autres approches de prévention du cancer cervical (frottis cervical et
test par ADN HPV), dont les bénéfices sont plus
élevés lorsque les femmes sont plus âgées lorsque
le pic typique d'acquisition du HPV et la clairance (c-à-d., >30
ans) sont pris pour cible de
l'évaluation.27
L'examen du niveau de bénéfice procuré par une
vaccination HPV des femmes qui ont passé leur pic d'exposition est
actuellement en cours d'évaluation dans plusieurs essais
d'efficacité clinique.
Il n'est également pas certain que la vaccination apporte un
bénéfice aux femmes ayant une infection prévalente en
augmentant leur résistance immunologique contre la réapparition
(via réactivation ou réinfection) du même type viral dans
le futur. Les femmes infectées par le HPV qui arrivent à
éliminer leur infection, ont démontré une
immunocompétence pour maîtriser une infection établie par
le HPV, ces femmes peuvent attendre et peuvent maîtriser des infections
ultérieures sans avoir besoin d'une vaccination. Il est possible en
particulier d'émettre l'hypothèse que les réponses aux
cellules T développées après une infection initiale par
le HPV qui disparaît par la suite, seraient capables d'éradiquer
de façon adéquate les infections virales ultérieures.
Ceci reste un problème pour les investigations futures.
Dans l'analyse actuelle, nous avons évité d'évaluer
les données cytologiques et/ou histologique obtenues après
randomisation car pouvant compromettre l'objectif initialement
déclaré de notre essai randomisé, à savoir
évaluer l'efficacité du vaccin HPV-16/18 pour protéger
les femmes sans infection HPV de développer des états
précancéreux de haut grade ou un cancer. Nous ne pouvons donc
éliminer formellement la possibilité que la vaccination
prévienne la progression d'une évolution histo-cytologique.
Toutefois, compte tenu que les taux de clairance virale ne diffèrent
pas en fonction du groupe de traitement et qu'une infection virale persistante
est le facteur prédictif le mieux documenté du risque de
progression, il est improbable que la vaccination puisse avoir un effet
significatif sur la vitesse de progression de la
lésion.1,17
L'essai étant en cours et les investigateurs et le personnel des
centres n'ayant pas accès aux données de tolérance selon
les groupes de traitement, nous avons aussi évalué le profil de
tolérance du vaccin dans cette analyse. Toutefois, les résultats
d'efficacité provenant de l'analyse présente mettent en garde
contre le bénéfice de la vaccination pour traiter les infections
établis, indépendamment du profil de tolérance.
Compte tenu des données publiées suggérant que la
tolérance globale du vaccin
actue1,3,28
la question résiduelle principale est de savoir si la
réactogenicité et les profils d'événements
indésirables diffèrent selon le statut de l'infection par le HPV
au moment de la vaccination. Les données destinées à
évaluer ces questions directement seront disponibles après la
levée de l'aveugle dans notre étude et dans les études en
cours.
Nous avons évalué la clairance virale à 6 et 12 mois
après inclusion. Alors que l'évaluation de la clairance virale
à 6 mois avait l'avantage d'inclure plus de 85% des participantes avec
une infection prévalente à l'inclusion par le HPV, elle jugeait
de l'efficacité avant que la série complète des
vaccinations soit administrée. Inversement, l'évaluation de la
clairance virale à 12 mois avait l'avantage de juger des taux de
clairance après la série complète de vaccinations, mais
incluait seulement un faible pourcentage (70%) de participantes ayant une
infection prévalente au HPV à l'inclusion. Il est rassurant de
noter que les résultats étaient compatibles dans les deux
approches.
Les résultats de notre étude basée sur une
communauté apportent des preuves solides qu'il y a peu, ou pas, de
bénéfice thérapeutique du vaccin dans la population que
nous avons étudiée. Par ailleurs, nous ne voyons pas de raison
de croire qu'il y ait ailleurs un bénéfice thérapeutique
du vaccin, car l'effet biologique de la vaccination chez des femmes
déjà infectées ne devrait par varier selon les
populations. Nous notons qu'alors que les estimations sur l'efficacité
du vaccin rapportées ici sont exactes, les estimations de la clairance
absolue dans les groupes individuels de l'étude peuvent être trop
élevées car nous avons exclus de l'analyse les femmes
orientées vers une colposcopie; les infections chez ces femmes ont sans
aucun doute moins de probabilité de disparaître que chez les
femmes qui n'ont pas été orientées vers une
colposcopie.
En résumé, nos résultats montrent que, chez des femmes
positives pour l'ADN du HPV, une vaccination HPV-16/18
n'accélère pas la clairance du virus et ne doit pas être
utilisée pour traiter les infections prévalentes.
Informations sur les auteurs
Correspondance: Allan Hildesheim, PhD, Division of Cancer Epidemiology
and Genetics, National Cancer Institute, 6120 Executive Blvd, Ste 550,
Rockville, MD 20852
(Hildesha{at}exchange.nih.gov);
Rolando Herrero, MD, PhD, Proyecto Epidemiolgico Guanacaste, Torre La Sabana,
300 Oeste del ICE, Piso 7, Sabana Norte, San José, Costa Rica
(Rherrero{at}amnet.co.cr).
Les affiliations des auteurs et une liste complète des
investigateurs du Costa Rican HPV Vaccine Trial Group sont
indiquées à la fin de cet article.
Contributions des auteurs: Les Drs Hildesheim, Herrero et Wacholder
ont eu un accès complet à toutes les données de
l'étude et acceptent la responsabilité de
l'intégrité et acceptent la responsabilité de
l'intégrité et de l'exactitude de l'analyse des
données.
Conception et schéma de l'étude: Hildesheim,
Herrero, Wacholder, Rodriguez, Bratti, Schiller, Dubin, Lowy.
Recueil des données: Hildesheim, Herrero, Rodriguez,
Solomon, Bratti, Gonzalez, Porras, Jimenez.
Analyse et interprétation des données: Hildesheim,
Herrero, Wacholder, Rodriguez, Solomon, Bratti, Schiller, Dubin, Lowy.
Rédaction du manuscrit: Hildesheim, Herrero, Schiller.
Revue critique du manuscrit: Hildesheim, Herrero, Wacholder,
Rodriguez, Solomon, Bratti, Schiller, Gonzalez, Dubin, Porras, Jimenez,
Lowy.
Analyse statistique: Hildesheim, Wacholder.
Obtention du financement: Hildesheim, Herrero, Dubin, Lowy.
Aide administrative, technique ou matérielle: Herrero,
Solomon, Bratti, Gonzalez, Porras, Jimenez
Supervision de l'étude: Hildesheim, Herrero, Solomon, Bratti,
Schiller.
Liens financiers: Les Drs Schiller et Lowy ont déclaré
qu'ils ont été considérés comme les inventeurs des
patentes du gouvernement des Etats-Unis du vaccin HPV, mais licenciées
par GSK et Merck et ont droit à des royalties limitées,
spécifiées par loi fédérale. Le Dr Dubin travaille
chez GSK Biologicals, le fabricant du vaccin de cette étude. Aucun
autre lien financier n'a été rapporté.
Costa Rican HPV Vaccine Trial Group: Proyecto Epidemiologico
Guanacaste, Fundación INCIENSA, San José, Costa Rica: Mario
Alfaro (cytologist), Manuel Barrantes (field supervisor), M. Concepcion Bratti
(coinvestigator), Fernando Cardenas (general field supervisor), Bernal
Cortés (specimen and repository manager), Albert Espinoza (head, coding
and data entry), Yenory Estrada (pharmacist), Paula Gonzalez (coinvestigator),
Diego Guillén (pathologist), Rolando Herrero (co-principal
investigator), Silvia E. Jimenez (trial coordinator), Jorge Morales
(colposcopist), Lidia Ana Morera (head study nurse), Elmer Pé rez
(field supervisor), Carolina Porras (co-investigator), Ana Cecilia Rodriguez
(co-investigator), Maricela Villegas (clinic physician); University of Costa
Rica, San José : Enrique Freer (director, HPV diagnostics laboratory),
Jose Bonilla (head, HPV immunology laboratory), Sandra Silva (head
microbiologist, HPV diagnostics laboratory), Ivannia Atmella (microbiologist,
immunology laboratory), Margarita Ramirez (microbiologist, immunology
laboratory); National Cancer Institute [NCI], Bethesda, Maryland: Pam Gahr
(trial coordinator), Allan Hildesheim (co-principal investigator and NCI
co-project officer), Douglas R. Lowy (HPV virologist), Mark Schiffman (medical
monitor and NCI co-project officer), John T. Schiller (HPV virologist), Mark
Sherman (quality control pathologist), Diane Solomon (medical monitor and
quality control pathologist), Sholom Wacholder (statistician); Science
Applications International Corporation, NCI-Frederick, Frederick, Maryland:
Ligia Pinto (head, HPV immunology laboratory), Alfonso Garcia-Pineres
(scientist, HPV immunology laboratory); Women and Infants Hospital of Rhode
Island, Providence: Claire Eklund (quality control cytology), Martha
Hutchinson (quality control cytology); Delft Diagnostics Laboratory, Delft,
the Netherlands: Wim Quint (HPV DNA testing), Leen-Jan van Doorn (HPV DNA
testing); Data and Safety Monitoring Board: Steven Self (chair) Luis Diego
Calzada, Ruth Karron, Ritu Nayar, Nancy Roach; Scientific HPV Working Group
(external): Joanna Cain (chair), Diane Davey, David DeMets, Francisco Fuster,
Ann Gershon, Elizabeth Holly, Silvia Lara, Raphael Viscidi, Henriette
Raventos, Luis Rosero-Bixby, Kristen Suthers.
Financement/Soutien : L'essai Costa Rican HPV Vaccine est un travail
de collaboration depuis longtemps entre les investigateurs du Costa Rica et le
NCI. L'essai est sponsorisé et financé par le NCI (bourse
N01-CP-11005), avec un financement du National Institutes of Health Office for
Research on Women's Health, et mené avec le soutien du Ministry of
Health of Costa Rica. Le vaccin était fourni pour notre étude
par GSK Biologicals, grâce à un Clinical Trials Agreement avec le
NCI. GlaxoSmithKline a également fourni un soutien pour tout ce qui
concernait les besoins de soumission administratifs de la compagnie par une
bourse FDA BB-IND 7920.
Rôle des sponsors : Les investigateurs NCI et Costa Rica sont
responsables du schéma et de la conduite de l'étude, du recueil,
de la gestion, de l'analyse et de l'interprétation des données
ainsi que de la préparation du manuscrit. Le NCI et les investigateurs
du Costa Rica ont pris les décisions finales éditoriales sur
cette publication et les autres ultérieures; GSK a le droit de revoir
et de commenter.
Autres contributions: Nous remercions les femmes de Guanacaste et
Puntarenas, Costa Rica, qui ont participé à l'étude. Nous
remercions aussi pour leur effort et leur dévouement le personnel du
Costa Rica impliqué dans ce projet, dont Bernardo Blanco et son
équipe (recensement); Ricardo Cerdas and Ana Hernandez (traitement des
échantillons sanguins); Osman Lopez, Johnny Matamoros, Cristian
Montero, Rafael Thompson, and Jorge Umana (coordinateurs de terrain); Su Yen
Araya, Hazel Barquero, Hayleen Campos, Muriel Grijalba, Ana Cristina Monge,
Ana Peraza, Diana Robles, Maria Fernanda Saenz, Dorita Vargas, et Jessica
Vindas (coordinateurs cliniques); Paola Alvarez, Dinia Angulo, Ana Live Arias,
Betzaida Barrantes, Marianela Bonilla, Jessenia Chinchilla, Marianela Herrera,
Andrea Interiano, Viviana Loria, Rebeca Ocampo, Angie Ramirez, Libia Rivas,
Jessenia Ruiz, Malena Salas, and Yesenia Vazquez (praticiens); Marta Alvarado,
Ana Cristina Arroyo, Gloriana Barrientos, Diana Diaz, Marlen Jara, Maureen
Matarrita, Maria Ester Molina, Elida Ordonez, Gina Sanchez, and Siara Villegas
(infirmières); Arianne Castrillo et Vivian Lopez (éducation et
coordinateurs de l'effort sur le terrain); Karla Coronado (coordinateur des
rendez-vous); Ricardo Alfaro (coordinateur du contrôle de
qualité); Charles Sanchez and Livia Romero (coordinateurs de centre de
documentation); Eric Alpizar et Carlos Avila (coordinateurs des technologies
d'information). Nous remercions particulièrement Sofia Elizondo,
directrice exécutive de la Fondation 'n INCIENSA, et son équipe
pour le soutien administratif. Nous remercions l'équipe des Information
Management Services, Silver Spring, Maryland, responsable du
développement et de la gestion du système de données
utilisé dans cet essai et qui ont agi comme le centre de prise en
charge des données de cet essai, en particulier Julie Buckland, Jean
Cyr, Laurie Rich, et John Schussler. Nous remercions les contributions
individuelles à Westat Inc, Rockville, Maryland, qui ont soutneu le
développement et ont suivi le projet, dont Maribel Gomez, Kirk Midkiff,
Kerrygrace Morrisey, et Susan Truitt. Nous remercions pour leur aide Carla
Chorley, Troy Moore, Kathi Shea, et Heather Siefers pour
l'établissement d'un dépôt pour les échantillons et
pour les vaccins et pour leur aide continue dans la manipulation et
l'acheminement des échantillons. Chez GSK Biologicals, nous remercions
Anne Schuind, Kelechi Lawrence, Darrick Fuet and Bruce Innis pour leur
contribution aux discussions concernant l'étude et Francis Dessy et
Brigitte Colau pour l'évaluation des anticorps HPV-16/18.
Affiliations des auteurs: Division of Cancer Epidemiology and
Genetics, Division of Cancer Prevention and Control, and Center for Cancer
Research, National Cancer Institute, Bethesda, Maryland; Proyecto
Epidemiologico Guanacaste, Fundacion INCIENSA, San José, Costa Rica;
GlaxoSmithKline Biologicals, King of Prussia, Pennsylvania.
BIBLIOGRAPHIE
 |  |
1. Schiffman MH, Hildesheim A. Cervical cancer. In: Schottenfeld D,
Fraumeni JFF Jr, eds. Cancer Epidemiology and
Prevention. Oxford, England: Oxford University Press;2006
: 1044-1067.
2. Villa LL, Costa RL, Petta CA, et al. Prophylactic quadrivalent
human papillomavirus (types 6, 11, 16, and 18) L1 viruslike particle vaccine
in young women: a randomized double-blind placebo-controlled multicentre phase
II efficacy trial. Lancet Oncol.2005; 6(5):271
-278.
PUBMED
3. Harper DM, Franco EL, Wheeler CM, et al. Sustained efficacy up to
4.5 years of a bivalent L1 virus-like particle vaccine against human
papillomavirus types 16 and 18: follow-up from a randomised control trial.
Lancet.2006; 367(9518):1247
-1255.
PUBMED
4. Garland SM, Hernandez-Avila M, Wheeler CM, et al. Quadrivalent
vaccine against human papillomavirus to prevent anogenital diseases.
N Engl J Med.2007; 356(19):1928
-1943.
PUBMED
5. Future II Study Group. Quadrivalent vaccine against human
papillomavirus to prevent high-grade cervical lesions. N Engl J
Med.2007; 356(19):1915
-1927.
PUBMED
6. Mao C, Koutsky LA, Ault KA, et al. Efficacy of human
papillomavirus-16 vaccine to prevent cervical intraepithelial neoplasia: a
randomized controlled trial. Obstet Gynecol.2006; 107(1):18
-27.
PUBMED
7. Stanley M, Lowy DR, Frazer I. Prophylactic HPV vaccines: underlying
mechanisms. Vaccine.2006; 24(suppl 3):S106
-S113.
PUBMED
8. Lowy DR, Schiller JT. Prophylactic human papillomavirus vaccines.
J Clin Invest.2006; 116(5):1167
-1173.
PUBMED
9. Nardelli-Haefliger D, Wirthnew D, Schiller JT, et al. Specific
antibody levels at the cervix are menstrual-cycle dependent in women
vaccinated with human papillomavirus type 16 virus like particles.
J Natl Cancer Inst.2003; 95(15):1128
-1137.
FREE FULL TEXT
10. Giannini SL, Hanon E, Moris P, et al. Enhanced humoral and memory B
cellular immunity using HPV16/18 L1 VLP vaccine formulated with the
MPL/aluminium salt combination (AS04) compared to aluminium salt only.
Vaccine.2006; 24(33-34):5937
-5949.
PUBMED
11. Villa LL, Ault KA, Giuliano AR, et al. Immunologic responses
following administration of a vaccine targeting human papillomavirus types 6,
11, 16, and 18 Vaccine.2006; 24(27-28):5571
-5583.
PUBMED
12. Pinto LA, Edwards J, Castle PE, et al. Cellular immune responses to
human papillomavirus (HPV)-16 L1 in healthy volunteers immunized with
recombinant HPV-16 L1 viruslike particles. J Infect
Dis.2003; 188(2):327
-338.
FREE FULL TEXT
13. Pinto LA, Castle PE, Roden RB, et al. HPV-16 L1 VLP vaccine elicits
a broad-spectrum of cytokine responses in whole blood.
Vaccine.2005; 23(27):3555
-3564.
PUBMED
14. Emeny RT, Wheeler CM, Jansen KU, et al. Priming of human
papillomavirus type 11-specific humoral and cellular immune responses in
college-aged women with a viruslike particle vaccine. J
Virol.2002; 76(15):7832
-7842.
FREE FULL TEXT
15. Peng S, Frazer IH, Fernando GJ, Zhou J. Papillomavirus viruslike
particles can deliver defined CTL epitopes to the MHC class I pathway.
Virology.1998; 240(1):147
-157.
PUBMED
16. Kirnbauer R, Chandrachud LM, O'Neil BW, et al. Viruslike particles
of bovine papillomavirus type 4 in prophylactic and therapeutic immunization.
Virology.1996; 219(1):37
-44.
PUBMED
17. Schiffman M, Herrero R, Desalle R, et al. The carcinogenicity of
human papillomavirus types reflects viral evolution.
Virology.2005; 337(1):76
-84.
PUBMED
18. Wright TC Jr, Schiffman M, Solomon D, et al. Interim guidance for
the use of human papillomavirus DNA testing as an adjunct to cervical cytology
for screening. Obstet Gynecol.2004; 103(2):304
-309.
PUBMED
19. Saslow D, Runowicz CD, Solomon D, et al. American Cancer Society
guideline for the early detection of cervical neoplasia and cancer.
CA Cancer J Clin.2002; 52(6):342
-362.
PUBMED
20. Atypical Squamous Cells of Undetermined Significance/Low-Grade
Squamous Intraepithelial Lesions Triage Study Group. Human papillomavirus
testing for triage of women with cytologic evidence of low-grade squamous
intraepithelial lesions: baseline data from a randomized trial. J
Natl Cancer Inst.2000; 92(5):397
-402.
FREE FULL TEXT
21. Kleter B, van Doorn LJ, Schrauwen L, et al. Development and
clinical evaluation of a highly sensitive PCR-reverse hybridization line probe
assay for detection and identification of anogenital human papillomavirus.
J Clin Microbiol.1999; 37(8):2508
-2517.
FREE FULL TEXT
22. Kleter B, van Doorn LJ, ter Schegget J, et al. Novel short-fragment
PCR assay for highly sensitive broad-spectrum detection of anogenital human
papillomaviruses. Am J Pathol.1998; 153(6):1731
-1739.
PUBMED
23. van Doorn LJ, Molijn A, Kleter B, Quint W, Colau B. Highly
effective detection of human papillomavirus 16 and 18 DNA by a testing
algorithm combining broad-spectrum and type-specific PCR. J Clin
Microbiol.2006; 44(9):3292
-3298.
FREE FULL TEXT
24. Baay MF, Quint WG, Koudstaal J, et al. Comprehensive study of
several general and type-specific primer pairs for detection of human
papillomavirus DNA by PCR in paraffin-embedded cervical carcinomas.
J Clin Microbiol.1996; 34(3):745
-747.
FREE FULL TEXT
25. Schachter J, Hook EW III, McCormack WM, et al. Ability of the
Digene Hybrid Capture II test to identify Chlamydia trachomatis and
Neisseria gonorrhoeae in cervical specimens. J Clin
Microbiol.1999; 37(11):3668
-3671.
FREE FULL TEXT
26. Liang KY, Zeger SL. Longitudinal data analysis using generalized
linear models. Biometrika.1986; 73:13
-22.
FREE FULL TEXT
27. Schiffman M, Castle PE. The promise of global cervical-cancer
prevention. N Engl J Med.2005; 353(20):2101
-2104.
PUBMED
28. Harper DM, Franco EL, Wheeler C, et al. Efficacy of a bivalent L1
viruslike particle vaccine in prevention of infection with human
papillomavirus types 16 and 18 in young women: a randomised controlled trial.
Lancet.2004; 364(9447):1757
-1765.
PUBMED
ARTICLES EN RAPPORT
Cette semaine dans le JAMA
JAMA. 2007;298:715.
Texte Complet
Les vaccins HPV—Prophylactiques, pas thérapeutiques
Lauri E. Markowitz
JAMA. 2007;298:805-806.
Texte Complet
|