 |
 |

Effet d'un régime riche en légumes, en fruits et en fibres, et pauvre en graisses, sur le pronostic après un traitement du cancer du seinÉtude randomisée WHEL (Women's Healthy Eating and Living)
John P. Pierce, PhD;
Loki Natarajan, PhD;
Bette J. Caan, DrPh;
Barbara A. Parker, MD;
E. Robert Greenberg, MD;
Shirley W. Flatt, MS;
Cheryl L. Rock, PhD, RD;
Sheila Kealey, MPH;
Wael K. Al-Delaimy, MD, PhD;
Wayne A. Bardwell, PhD;
Robert W. Carlson, MD;
Jennifer A. Emond, MS;
Susan Faerber, BA;
Ellen B. Gold, PhD;
Richard A. Hajek, PhD;
Kathryn Hollenbach, PhD;
Lovell A. Jones, PhD;
Njeri Karanja, PhD;
Lisa Madlensky, PhD;
James Marshall, PhD;
Vicky A. Newman, MS, RD;
Cheryl Ritenbaugh, PhD, MPH;
Cynthia A. Thomson, PhD;
Linda Wasserman, MD, PhD;
Marcia L. Stefanick, PhD
RÉSUMÉ
 |  |
Contexte Il existe peu de données soutenant qu'un
régime alimentaire riche en légumes, en fruits et en fibres, et
pauvre en graisse totale peut avoir un impact sur la récidive du cancer
du sein ou la survie.
Objectif Déterminer si une augmentation majeure de la
consommation de légumes, de fruits et de fibres, parallèlement
à une diminution de l'apport en graisses alimentaires, réduit le
risque de récidive et de nouveau cancer du sein primaire, ainsi que la
mortalité toutes causes confondues chez des femmes avec un cancer du
sein précédemment traité au stade précoce.
Schéma, cadre et participants Étude
contrôlée randomisée multicentrique sur le changement
alimentaire, menée chez 3 088 femmes précédemment
traitées pour un cancer du sein au stade précoce,
âgées de 18 à 70 ans au moment du diagnostic. Les femmes
ont été recrutées entre 1995 et 2000 et suivies jusqu'au
1er juin 2006.
Intervention Le groupe d'intervention (n = 1 537) a
été aléatoirement assigné à recevoir un
programme de conseils téléphoniques complété par
des séances culinaires et des lettres d'information promouvant des
objectifs quotidiens de 5 portions de légumes plus 500 ml de jus de
légume; 3 portions de fruits; 30 g de fibres; et 15 % à 20 %
d'apport énergétique en graisses. Le groupe de comparaison (n =
1 551) recevait des matériels imprimés décrivant le
programme alimentaire « 5 par Jour ».
Principaux critères d'évaluation Survenue de cancer du
sein invasif (récidive ou nouveau cancer primaire) ou
décès toutes causes confondues.
Résultats À partir de régimes alimentaires
initiaux comparables, une analyse d'imputation conservatrice a montré
que le groupe d'intervention vs groupe de comparaison obtenait les
différences statistiquement significatives suivantes, qui
étaient soutenues pendant 4 ans: portions de légumes, +65 %;
fruits, + 25%; fibres, +30 %, et apport énergétique en graisses,
-13 %. Les concentrations plasmatiques de caroténoïde
étaient mesurées pour valider les changements rapportés
dans la consommation de fruits et légumes. Tout au long de
l'étude, les femmes des deux groupes recevaient des soins cliniques
similaires. Sur le suivi moyen de 7,3 ans, 256 femmes du groupe d'intervention
(16,7 %) vs 262 du groupe de comparaison (16,9 %) ont présenté
un cancer du sein invasif (risque relatif ajusté, 0,96; intervalle de
confiance à 95 %, 0,80-1,14; p = 0,63), et 155 femmes du groupe
d'intervention (10,1 %) vs 160 femmes du groupe de comparaison (10,3 %) sont
décédées (risque relatif ajusté, 0,91; intervalle
de confiance à 95 %, 0,72-1,15; p = 0,43). Aucune interaction
significative n'a été observée entre le groupe de
régime et les données démographiques, les
caractéristiques de la tumeur initiale, le régime alimentaire
initial, ou le traitement du cancer du sein.
Conclusion Parmi les femmes survivant d'un cancer du sein au stade
précoce, l'adoption d'un régime à forte composante en
légumes, fruits et fibres et à faible teneur en graisses n'a pas
réduit la survenue de nouveau cancer du sein ou la mortalité
pendant une période de suivi de 7,3 ans.
TrialRegistration
clinicaltrials.govIdentifier:NCT00003787
JAMA.
2007;298(3):289-298
DDe nombreuses données d'études précliniques
indiquent que les aliments d'origine végétale contiennent des
anticarcinogènes.1
Une revue exhaustive de la littérature a démontré qu'un
régime riche en légumes et en fruits était susceptible de
réduire le risque de cancer du sein, et qu'un régime riche en
graisse totale augmentait potentiellement ce
risque.2
Cependant, les données démontrant une association entre un
régime riche en légumes et en fruits et pauvre en graisse
totale, et la prévention de la progression du cancer sont
contradictoires dans les études
épidémiologiques.3-17
Une analyse intermédiaire des données de l'étude WINS
(Women's Intervention Nutrition Study), qui évaluait l'effet d'une
intervention alimentaire destinée à réduire l'apport en
graisse sur la survie sans récidive chez des patientes avec cancer du
sein,18 a
trouvé que l'intervention était associée à une
amélioration marginalement statistiquement significative de la survie
sans récidive. À notre connaissance, aucune autre étude
clinique évaluant le changement alimentaire et la survie dans le cancer
du sein n'a été rapportée.
L'étude WHEL (Women's Healthy Eating and Living) était une
étude randomisée visant à déterminer si un
régime alimentaire très riche en légumes, en fruits et en
fibres et pauvre en graisses réduisait les risques de récidive
et de nouveau cancer du sein primaire, ainsi que la mortalité toutes
causes confondues chez les femmes avec un cancer du sein au stade
précoce précédemment traité. L'étude
était basée sur les recommandations d'un comité national
d'experts, convoqué pour répondre à une subvention
défi offerte en 1993 par un philanthrope privé, qui pensait que
le rôle du régime alimentaire dans la prévention de la
progression du cancer méritait une étude scientifique, afin de
permettre aux survivants de la maladie de prendre des décisions sans
devoir uniquement « se fier au mythe, aux rumeurs et aux on-dit
».19
MÉTHODES
Les détails du schéma de l'étude, des critères
d'éligibilité, des procédures de randomisation et des
interventions alimentaires ont été rapportés
précédemment.20,21
En bref, nous avons comparé 2 régimes alimentaires: un groupe
d'intervention qui recevait des conseils intensifs pour adopter un
régime alimentaire à forte composante en légumes, en
fruits et en fibres, et pauvre en
graisses,21
et un groupe de comparaison auquel il était conseillé de suivre
le programme de « 5 par jour
».22,23
L'étude testait des hypothèses primaires visant à
déterminer si le régime alimentaire d'intervention était
associé
à1 un
délai plus long sans survenue de cancer du sein, et
à2 une
augmentation de la survie globale chez les femmes précédemment
traitées pour un cancer du sein au stade précoce. Sur la base de
6 études épidémiologiques qui avaient été
publiées au moment de l'élaboration de l'étude, nous
avons estimé la taille d'effet probable de ce régime à
composantes
multiples.20
D'après Lachin et
Foulkes,24
nous avons déterminé qu'une taille d'échantillon de 3 000
patients fournirait une puissance de 82 % pour détecter une
réduction de 19 % des survenues de cancer du sein dans le groupe
d'intervention (taux attendu dans le groupe de comparaison = 24 %), et une
réduction de 24 % de la mortalité toutes causes confondues (taux
attendu dans le groupe de comparaison = 15 %).
Participants
Les participants ont été recrutés dans 7 centres,
entre 1995 et 2000. Les critères d'éligibilité incluaient
le diagnostic de cancer du sein primaire invasif opérable,
classifié selon les critères de l'American Joint Committee on
Cancer (Edition IV) en stade I (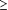 1 cm), stade II ou stade IIIA, dans les 4
dernières années; un âge de 18 à 70 ans au moment
du diagnostic; le traitement par curage axillaire et mammectomie totale ou
exérèse locale de la tumeur du sein, suivie par une
radiothérapie du sein; l'absence de chimiothérapie actuelle ou
prévue; l'absence de signe de maladie récidivante ou de nouveau
cancer du sein depuis l'achèvement du traitement local initial; et
l'absence d'autre cancer au cours des 10 dernières années. Les
femmes éligibles étaient assignées aléatoirement
au régime alimentaire de l'étude ou au groupe de comparaison
(Figure 1). Les comités
d'éthique des 7 centres investigateurs ont approuvé le protocole
de l'étude et les formulaires de consentement, et tous les participants
ont donné leur consentement éclairé écrit. 1 cm), stade II ou stade IIIA, dans les 4
dernières années; un âge de 18 à 70 ans au moment
du diagnostic; le traitement par curage axillaire et mammectomie totale ou
exérèse locale de la tumeur du sein, suivie par une
radiothérapie du sein; l'absence de chimiothérapie actuelle ou
prévue; l'absence de signe de maladie récidivante ou de nouveau
cancer du sein depuis l'achèvement du traitement local initial; et
l'absence d'autre cancer au cours des 10 dernières années. Les
femmes éligibles étaient assignées aléatoirement
au régime alimentaire de l'étude ou au groupe de comparaison
(Figure 1). Les comités
d'éthique des 7 centres investigateurs ont approuvé le protocole
de l'étude et les formulaires de consentement, et tous les participants
ont donné leur consentement éclairé écrit.
|
|

|
|
Figure 1.. Organigramme des participants
|
|
|
Intervention alimentaire
L'intervention intensive était essentiellement
délivrée sous forme de conseils téléphoniques,
complétés par 12 séances culinaires dans la
première année et de lettres d'information mensuelles tout au
long de l'étude. Les conseillers
expérimentés21
suivaient un protocole assisté par ordinateur, basé sur une
théorie cognitive
sociale25 et
comportant 3 phases d'intensité décroissante. Pendant la
première phase (3-8 appels téléphoniques en 4-6
semaines), les conseillers se focalisaient sur le développement d'une
autodiscipline pour l'accomplissement des objectifs de l'étude, qui
consistaient en une consommation quotidienne de 5 portions de légumes
plus 500 ml de jus de légume, de 3 portions de fruits, de 30 g de
fibres, et 15% à 20 % d'apport énergétique en graisses.
La phase 2 (jusqu'au 5ème mois) était axée sur
l'autosurveillance et traitait les obstacles à l'observance. La phase 3
(jusqu'à la fin de l'étude) était axée sur le
maintien de la motivation dans le suivi du régime alimentaire de
l'étude et la prévention des rechutes. Pendant la
première année de l'intervention, les participants ont
reçu une moyenne de 18 séances de conseils
téléphoniques, assisté à une moyenne de 4
séances culinaires sur les 12 proposées, et reçu 12
lettres d'information de l'étude. À 4 ans, temps
d'évaluation clé pour l'effet à long terme de
l'intervention, ces participants avaient reçu une moyenne de 31 appels
téléphoniques et 48 lettres d'information.
Les femmes randomisées dans le groupe de comparaison recevaient des
matériels imprimés (édités par le ministère
américain de
l'agriculture26
et le National Cancer
Institute22,23)
décrivant un régime avec un apport quotidien recommandé
de 5 portions de légumes et de fruits, plus de 20 g de fibres et moins
de 30 % d'apport énergétique total en graisse. Le groupe de
comparaison a assisté en moyenne à 1 des 4 séances
culinaires proposées dans la première année, et
reçu 24 lettres d'information conçues pour ce groupe pendant les
4 premières années.
Recueil des données
Évaluation alimentaire. L'apport alimentaire était
évalué par des ensembles prédéfinis de 4 rappels
alimentaires de 24 heures, menés par téléphone à
des jours aléatoires sur une période de 3 semaines,
stratifiée pour les week-ends vs jours de la
semaine.20
Ces rappels alimentaires étaient prévus pour tous les
participants, à l'inclusion, à 1 an, 4 ans, et 6 ans, et sur un
échantillon aléatoire de 50 % à 6, 24 et 36 mois. Nous
rapportons les données des participants ayant achevé les
évaluations de suivi. Nous avons également mené les
analyses complémentaires suivantes: pour les participants n'ayant pas
achevé les évaluations de suivi, nous avons imputé des
estimations en supposant qu'ils avaient changé de régime
alimentaire de manière similaire aux répondeurs du groupe de
comparaison, en utilisant l'algorithme EM (Estimation-Maximisation) du
logiciel SAS, version 9.1 (SAS Institute Inc, Cary, Caroline du
Nord).27
Comme décrit
précédemment,20
les évaluateurs, après avoir suivi un programme de formation,
utilisaient le protocole de rappel informatique multipassage du logiciel NDS-R
(Nutritional Data System, 1994-2006, Université du Minnesota,
Minneapolis). Pour évaluer l'adhésion globale, nous avons
élaboré un score d'observance.20 Un participant
entièrement observant devait totaliser un score de 600 points: 300
points correspondaient à la consommation de légumes, et les 300
autres étaient divisés en parts égales entre les fibres,
les fruits, et l'apport énergétique en graisses.
Recueil d'autres données. Nous avons recueilli les
détails des antécédents familiaux de cancer à
l'inclusion, et avons utilisé les tableaux de prévalence des
mutations des laboratoires Myriad Genetic (Salt Lake City,
Utah)28 pour
classifier les familles ayant au moins un risque de 10 % de mutation du
gène BRCA1/2 comme étant à risque élevé.
Les visites de suivi effectuées à l'inclusion, à 1 an,
à 2 ou 3 ans (déterminée aléatoirement), et
à 4 ans et 6 ans incluaient la mesure du poids et une ponction
veineuse. Les échantillons sanguins ont été
stockés séparément dans des cryovals placés dans
des congélateurs à -80°C pour analyse ultérieure. Les
participants recevaient par courrier un ensemble de questionnaires à
compléter et à rapporter à chaque visite, incluant un
questionnaire de santé portant sur les récentes consultations de
médecin, et 2 questionnaires utilisés dans l'étude WHI
(Women's Health Initiative): un questionnaire sur les habitudes
personnelles,29
qui incluait une évaluation de 9 items sur l'activité physique
validée pour notre
étude,30
à partir de laquelle nous avons calculé l'équivalent
métabolique (MET) des minutes d'activité par
semaine,31
et un questionnaire sur les réflexions et les impressions
personnelles,32
qui incluait des évaluations du fonctionnement psychosocial. Chaque
participant rapportait sa race/ethnicité dans 1 des 8
catégories.
Évaluation des critères étudiés
Les critères primaires d'évaluation
étaient1
le critère combiné de récidive de cancer du sein invasif
ou nouveau cancer du sein primaire
et2 la
mortalité de toute cause. Les récidives étaient en outre
classifiées en métastases locales/régionales ou à
distance. Le carcinome in situ n'était pas considéré
comme un critère de l'étude. L'intervalle sans survenue de
cancer du sein était défini par le délai entre la date de
recrutement et le développement d'un nouveau cancer du sein. Le temps
de suivi était censuré au décès du participant,
à la date des dernières nouvelles, ou à la date
d'achèvement de l'étude (1er juin 2006).
Au cours des entretiens téléphoniques semestriels, le
personnel du centre investigateur interrogeait les participants sur la
survenue des événements évalués, sur une
éventuelle hospitalisation, ou sur les diagnostics médicaux
nouveaux ou existants. Tout rapport de cancer du sein ou de
décès motivait un entretien de confirmation et le recueil des
dossiers médicaux et/ou des certificats de décès. Deux
oncologues indépendants passaient en revue les dossiers médicaux
(rapports pathologiques et notes des médecins) pour confirmer les
récidives rapportées. En cas de désaccord, le
pathologiste du centre coordonnateur jugeait l'événement. Enfin,
nous avons effectué une recherche dans le registre national des
décès en utilisant le numéro de sécurité
sociale, le nom et la date de naissance des patients.
Analyse statistique
Les participants ont été assignés aléatoirement
au groupe d'intervention ou de comparaison à l'aide d'un schéma
de blocs de permutation aléatoires, stratifié par stade tumoral,
âge, et centre. L'assignation des participants était
effectuée par le centre coordonnateur, en utilisant le programme
informatique de randomisation de l'étude qui entrait automatiquement le
groupe attribué dans la base de données. Un comité
indépendant de surveillance des données a revu en aveugle les
exclusions post-randomisation
potentielles.20
Les comparaisons intergroupes initiales des données
démographiques, anthropométriques et cliniques, ainsi que des
critères alimentaires, ont été effectuées par
tests t bilatéraux, tests de Mann-Whitney ou  2. Nous
avons basé l'analyse primaire de la survie sans maladie sur le principe
de l'intention de traiter, en utilisant des techniques d'analyse de survie. Un
test du log-rank bilatéral a été effectué, avec
une valeur de p < 0,041 considérée comme statistiquement
significative (pour prendre en compte les analyses intermédiaires
effectuées à la demande du comité de surveillance des
données). Les risques relatifs ajustés et non ajustés ont
été et un modèle de Cox stratifié sur le stade
tumoral, l'âge et le centre a été construit. La
fréquence d'utilisation d'un traitement antiœstrogène et
des ovariectomies bilatérales différait marginalement entre les
groupes à l'inclusion; ces covariables ont donc également
été incluses dans le modèle. Cependant, la variable
traitement antiœstrogène ne satisfaisait pas à
l'hypothèse des risques proportionnels ; l'analyse a donc
été stratifiée sur cette
covariable.33
Ainsi, le modèle final était stratifié sur le stade de la
tumeur initiale, l'âge à la randomisation, le centre
investigateur et l'utilisation d'antiœstrogènes, et ajusté
sur le statut d'ovariectomie. 2. Nous
avons basé l'analyse primaire de la survie sans maladie sur le principe
de l'intention de traiter, en utilisant des techniques d'analyse de survie. Un
test du log-rank bilatéral a été effectué, avec
une valeur de p < 0,041 considérée comme statistiquement
significative (pour prendre en compte les analyses intermédiaires
effectuées à la demande du comité de surveillance des
données). Les risques relatifs ajustés et non ajustés ont
été et un modèle de Cox stratifié sur le stade
tumoral, l'âge et le centre a été construit. La
fréquence d'utilisation d'un traitement antiœstrogène et
des ovariectomies bilatérales différait marginalement entre les
groupes à l'inclusion; ces covariables ont donc également
été incluses dans le modèle. Cependant, la variable
traitement antiœstrogène ne satisfaisait pas à
l'hypothèse des risques proportionnels ; l'analyse a donc
été stratifiée sur cette
covariable.33
Ainsi, le modèle final était stratifié sur le stade de la
tumeur initiale, l'âge à la randomisation, le centre
investigateur et l'utilisation d'antiœstrogènes, et ajusté
sur le statut d'ovariectomie.
Le plan d'analyse prédéfini20 incluait l'utilisation d'un
modèle de Cox (à risques proportionnels) pour évaluer
l'effet de l'intervention sur les principales covariables. Ces
dernières incluaient le stade de la maladie (classifié en I, II
ou III), l'âge à la randomisation (< 55 ans vs 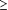 55 ans),
les caractéristiques des récepteurs hormonaux dans la tumeur
initiale, l'indice de masse corporelle, et le nombre d'années entre le
diagnostic et la randomisation. Les termes d'interaction entre le groupe de
randomisation et les variables indicatrices des catégories de
covariables ont été inclus dans les modèles de
régression de Cox. La signification des interactions entre le groupe de
randomisation et chaque covariable a été testée dans les
règles par tests du rapport de vraisemblance. Les résultats sont
présentés en rapports des risques proportionnels (risques
relatifs) et intervalles de confiance à 95%. 55 ans),
les caractéristiques des récepteurs hormonaux dans la tumeur
initiale, l'indice de masse corporelle, et le nombre d'années entre le
diagnostic et la randomisation. Les termes d'interaction entre le groupe de
randomisation et les variables indicatrices des catégories de
covariables ont été inclus dans les modèles de
régression de Cox. La signification des interactions entre le groupe de
randomisation et chaque covariable a été testée dans les
règles par tests du rapport de vraisemblance. Les résultats sont
présentés en rapports des risques proportionnels (risques
relatifs) et intervalles de confiance à 95%.
Dans les analyses complémentaires, nous avons examiné les
interactions potentielles entre le groupe de l'étude et les composantes
alimentaires initiales ciblées par l'intervention (légumes,
fruits, fibres, et apports en graisse) pour déterminer si les effets de
l'intervention alimentaire pouvaient varier en fonction du niveau de
consommation initial.
Les analyses ont été effectuées à l'aide du
progiciel statistique R, version 2.3.1 (R Foundation, Vienne, Autriche ;
http://www.r-project.org)
ou du logiciel
RÉSULTATS
Recrutement et caractéristiques initiales
L'équipe de recherche clinique a présélectionné
7 572 participants potentiels et en a randomisé 3 107, entre mars 1995
et le 30 novembre 2000 (Figure
1). Aucune différence n'a été relevée
dans les exclusions post-randomisation des deux groupes (9 vs 10).
L'échantillon final incluait 1 537 femmes dans le groupe d'intervention
alimentaire et 1 551 dans le groupe de comparaison.
La date de fin d'étude était le 1er juin 2006. Le nombre et
la fréquence des consultations médicales rapportées ne
différaient pas significativement entre les groupes, à tous les
temps d'évaluation de l'étude. Nous avons confirmé le
statut vital des participants à la date de fin d'étude
(Figure 1) pour 95 % du groupe
d'intervention et 96 % du groupe de comparaison. Le statut de cancer du sein
était confirmé pour 96 % du groupe d'intervention et 97 % du
groupe de comparaison.
La randomisation a produit des groupes fortement comparables
(Tableau 1) en termes de
données démographiques (âge, appartenance à une
minorité ethnique, et niveau d'instruction), de caractéristiques
du cancer du sein (stade, grade, atteinte ganglionnaire, statut des
récepteurs hormonaux, délai entre le diagnostic de cancer du
sein et la randomisation, et éligibilité pour l'analyse des
gènes BRCA1/2), et de traitement (chirurgie et radiothérapie par
exemple). De légers déséquilibres ont été
observés entre les groupes dans l'ovariectomie bilatérale,
l'usage d'antiœstrogènes et la chimiothérapie, qui
étaient tous en faveur d'un effet de l'intervention; cependant, aucune
différence intergroupe n'a été observée dans le
pourcentage de femmes ayant reçu au moins 1 de ces traitements
(intervention, 93,6 %; comparaison, 92,3 %; p = 0,12). Quatorze pour cent des
femmes se sont identifiées comme issues de minorités
raciales/ethniques; ces femmes étaient relativement également
réparties entre Afro-Américaines, Hispaniques et
Asiatiques.20
|
|

|
|
Tableau 1.. Caractéristiques initiales des participants à l'étude
WHEL par groupe étudiéa
|
|
|
Changements alimentaires entre groupes
Dans les analyses du changement alimentaire, seuls les participants sans un
critère de l'étude au moment de l'évaluation
étaient inclus. Une proportion élevée de femmes a
terminé les évaluations du régime alimentaire
(Tableau 2). À
l'inclusion, aucune différence intergroupe n'était
observée dans la consommation de légumes, de fruits ou de fibres
ou dans l'apport énergétique en graisses, les deux groupes
consommant une moyenne quotidienne de plus de 7 portions de fruits et
légumes. Aucune différence Dans le groupe de comparaison, la
consommation de légumes, de fruits ou de fibres ne variait que
modestement au cours des 6 années suivant la randomisation, tandis que
l'apport énergétique relatif en graisses augmentait de 13 %,
reflétant une tendance séculaire établie (J.P.P., V.A.N.,
L.N. et coll., données non publiées, mai 2007). Dans le groupe
d'intervention, le régime alimentaire changeait substantiellement, et
une importante différence intergroupe (p < 0,001) était
obtenue et maintenue pour chaque composante alimentaire, sur les 6
années de l'intervention. De l'absence de différence à
l'inclusion, le score d'observance global devenait supérieur de 91 %
dans le groupe d'intervention vs groupe de comparaison à 6 mois, et
restait supérieur de 61 % à 6 ans. Les détails des
changements dans les composantes alimentaires ciblées sont
présentés par ailleurs (J.P.P., V.A.N., L.N. et coll.,
données non publiées, mai 2007). Avec la méthode plus
conservatrice d'imputation des données, 27 le groupe d'intervention
avait augmenté sa consommation moyenne totale de fruits et de
légumes à 12 portions/j à 1 an. Ce changement dans la
consommation totale de fruits et légumes reflétait une
augmentation majeure dans la consommation de légumes, qui atteignait
une moyenne de 7,8 portions/j à 1 an et restait relativement
élevée, à 6 portions/j, au suivi de 4 ans. À 4
ans, les différences relatives dans la consommation moyenne entre les
groupes étaient de +65 % pour les portions de légumes, +25 %
pour les portions de fruits, +30 % pour les fibres, et -13 % pour l'apport
énergétique en lipides. Toutes les différences
étaient statistiquement significatives à un seuil de p <
0,001. La concentration plasmatique totale de caroténoïde, qui est
un biomarqueur de la consommation de fruits et légumes, était
supérieure de 73 % dans le groupe d'intervention vs groupe de
comparaison à 1 an, et supérieure de 43 % à 4 ans; ces
différences étaient statistiquement significatives (p <
0,001). En outre, une étude en sous-groupes a indiqué des
changements dans les concentrations plasmatiques de triglycérides et de
HDL (high-density lipoprotein)-cholestérol spécifiques au groupe
d'intervention, validant changements auto-rapportés dans les apports en
glucides et en
lipides.34
Les groupes présentaient une différence de moins de 80 kcal/j
dans l'apport énergétique et de moins de 1 kg dans le poids
corporel, à tous les temps de l'étude.
|
|

|
|
Tableau 2.. Régime alimentaire et poids corporel par groupea
|
|
|
|
|

|
|
Figure 2.. Estimation de Kaplan-Meier de la survie sans maladie et de la
mortalité toutes causes confondues par groupe de régime
|
|
|
Survie sans survenue de cancer du sein
Au cours de l'étude, 518 participants ont présenté un
cancer du sein (Tableau 3),
soit 256 (16,7 %) dans le groupe d'intervention et 262 (16,9 %) dans le groupe
de comparaison. Les courbes de survie sans maladie étaient pratiquement
identiques dans les 2 groupes (Figure
2). Le risque relatif non ajusté est présenté
dans la Figure 2. Le risque
relatif après ajustement sur l'utilisation
d'antiœstrogènes, le statut d'ovariectomie, et les facteurs de
stratification (incluant le stade tumoral, le centre et l'âge) à
l'inclusion était de 0,96 (intervalle de confiance à 95 %,
0,80-1,14; p = 0,63). Les statistiques du test du rapport de vraisemblance
pour les interactions du groupe avec l'âge, l'indice de masse
corporelle, l'activité physique, l'apport énergétique,
les caractéristiques de la tumeur initiale (incluant le statut des
récepteurs hormonaux), et le nombre d'années entre le diagnostic
et l'inclusion dans l'étude, n'étaient pas significatives
(Tableau 4). Les hazard ratio
pour les effets de l'intervention dans les strates des covariables
n'étaient pas non plus significatifs
(Tableau 4).
|
|

|
|
Tableau 3.. Événements de l'étude
|
|
|
|
|

|
|
Tableau 4.. Effets de l'intervention sur la survenue de nouveaux cancers du sein en
fonction des caractéristiques cliniques et démographiques
initiales
|
|
|
Mortalité globale
Trois cent quinze décès ont été
rapportés pendant la période de l'étude, dont 155 (10,1
%) dans le groupe d'intervention et 160 (10,3 %) dans le groupe de comparaison
(Figure 2). Plus de 80 % de la
totalité des décès étaient dus au cancer du sein
(Tableau 3). Le risque relatif
associé au traitement était de 0,91 (intervalle de confiance
à 95 %, 0,72-1,15; p = 0,43) après ajustement sur l'usage
d'antiœstrogènes, l'ovariectomie bilatérale et les
facteurs de stratification. Les statistiques du test du rapport de
vraisemblance pour les interactions du groupe avec l'âge, l'indice de
masse corporelle, l'activité physique, l'apport
énergétique, les caractéristiques de la tumeur initiale
(incluant le statut des récepteurs hormonaux), et les années
entre le diagnostic et l'entrée dans l'étude n'étaient
pas statistiquement significatives, pas plus que les effets de l'intervention
sur la mortalité, observés dans tous les sous-groupes de femmes
classifiées par covariables principales
(Tableau 5).
|
|

|
|
Tableau 5.. Effets de l'intervention sur la mortalité toutes causes confondues
en fonction des caractéristiques démographiques et cliniques
initiales
|
|
|
Effets du groupe en fonction des quartiles de consommation alimentaire à l'inclusion
Dans chaque quartile des composantes alimentaires ciblées, le groupe
d'intervention est parvenu à un changement significatif par rapport
à l'inclusion (Tableau
6). Cependant, aucune donnée ne démontrait de profil
cohérent d'effet de l'intervention sur la survenue de cancer du sein ou
sur la mortalité en fonction du sous-groupe de régime initial,
et les résultats statistiquement significatifs dans 2 des 40 strates
comparées sont ceux attendus du hasard.
|
|

|
|
Tableau 6.. Effets de l'intervention sur la survenue de nouveaux cancers du sein et la
mortalité toutes causes confondues en fonction des quartiles initiaux
d'apport alimentaire
|
|
|
COMMENTAIRES
 |  |
Dans cette étude randomisée sur une intervention alimentaire
visant à produire un changement substantiel en faveur d'un
régime très riche en légumes, en fruits et en fibres, et
pauvre en lipides, le risque de développer un nouveau cancer du sein et
la survie n'étaient pas modifiés chez les femmes
précédemment traitées au stade précoce de la
maladie. Aucun bénéfice significatif dans la récidive n'a
été globalement observé dans les sous-groupes de patients
définis par les données démographiques, le régime
initial, ou le type de tumeur initiale. Bien que les taux de mortalité
du cancer du sein aient diminué aux États-Unis pendant la
période de l'étude, 35 la similarité dans les profils de
survie entre les groupes de l'étude WHEL suggère qu'un suivi
continu ne modifierait pas les résultats observés.
Il est peu probable que nos résultats aient été
matériellement affectés par un biais dans l'évaluation
des principaux critères étudiés. Le suivi des
participants était presque complet et ne différait pas entre les
groupes, et nous n'avons pris en compte que les déclarations de
récidive et de nouvelles tumeurs primaires validées par une
revue du dossier médical. Nous avons observé des
différences intergroupes majeures et soutenues dans la consommation de
fruits et légumes, évaluée par les déclarations
des participants et les concentrations plasmatiques de
caroténoïde, marqueur biologique de la consommation de fruits et
légumes. Nous avons également observé des
différences significatives dans l'apport de fibres et de lipides. Bien
que le poids corporel ait été associé à la
santé, nous avons observé une différence de moins de 1 kg
dans le poids moyen entre les groupes de l'étude WHEL, à tous
les temps d'évaluation. Bien que des facteurs psychosociaux aient
été associés à la santé, nous n'avons
trouvé aucune différence intergroupe en matière de
dépression, de soutien social ou de qualité de vie pendant la
première année, lorsque l'intervention était la plus
intense.36 En conséquence, nous pensons que notre investigation
constitue une analyse adéquate de la capacité du régime
alimentaire étudié (très riche en légumes, en
fruits et en fibres, et pauvre en graisses) à produire un
bénéfice additionnel comparé au régime alimentaire
des femmes du groupe de comparaison. De nombreux participants de
l'étude WHEL avaient probablement modifié leur régime
alimentaire après avoir reçu leur diagnostic de cancer du
sein37; 75 %
consommaient au moins 5 portions de légumes et de fruits par jour
à la randomisation, ce qui est significativement supérieur au
niveau observé dans d'autres populations de survivantes du cancer du
sein.38,39
Cependant, nous avons observé peu de données indiquant un
bénéfice sur la récidive dans le quartile du groupe
d'intervention qui consommait moins de 5 portions de légumes et de
fruits à l'inclusion, malgré un changement majeur dans le
régime alimentaire, spécifique au groupe d'intervention.
Précédemment, dans des analyses longitudinales du groupe de
comparaison seul, nous avions observé un effet de seuil potentiel sur
la récidive pour les faibles concentrations plasmatiques initiales de
caroténoïde;13
nous avions également observé qu'une combinaison initiale de 5
fruits et légumes par jour et une activité physique
équivalant à une marche à un rythme modéré
pendant 30 minutes, 6 jours/semaine, était associée à une
moindre
mortalité.14
Cependant, dans cette analyse des données de l'étude
randomisée, une augmentation majeure de la consommation comparée
au régime alimentaire de « 5 par Jour » n'était pas
associée à une réduction des cancers du sein ou de la
mortalité. Nous suggérons une certaine réserve dans
l'application de nos résultats à des groupes de femmes autres
que celles représentées dans notre étude, qui se limitait
aux patientes ayant déjà eu un traitement initial du cancer du
sein, et excluait les femmes diagnostiquées après l'âge de
70 ans, de même que celles ayant des tumeurs de stade I de moins de 1
cm. En outre, seulement 14 % des femmes de notre population d'étude se
sont déclarées comme issues des groupes raciaux/ethniques
afro-américains, hispaniques et asiatiques.
Notre observation selon laquelle la réduction de l'apport en graisse
alimentaire ne produisait pas de bénéfice sur le pronostic du
cancer du sein se révèle en désaccord avec les analyses
intermédiaires de l'étude WINS (Women's Intervention Nutrition
Study), concluant que la réduction de l'apport en graisse alimentaire
était marginalement associée à une survie sans
récidive plus longue chez les patientes avec cancer du sein; cet effet
était plus souvent noté dans le sous-groupe de tumeurs
négatives pour les récepteurs aux œstrogènes.
Cependant, le suivi différentiel entre les groupes de l'intervention et
de comparaison peut avoir influencé le résultat de
l'étude WINS.40 En outre, la réduction du poids corporel
observée uniquement dans le groupe d'intervention peut être
partiellement responsable de l'amélioration de la survie sans rechute
dans l'étude WINS.41 Par ailleurs, bien que cette étude ait
rapporté une différence intergroupe de 8 % à 9 % dans
l'apport énergétique en graisse, maintenue pendant 5 ans, elle a
rapporté un taux supérieur de données manquantes
relatives à l'apport alimentaire dans le groupe d'intervention. Au
temps d'évaluation de 3 ans, les données étaient
disponibles pour 67 % du groupe d'intervention vs 74 % du groupe de
comparaison. À 5 ans, les données étaient disponibles
pour 39 % du groupe d'intervention et 44 % du groupe de comparaison. Si
même des proportions modérées de non-répondeurs
avaient augmenté leur consommation de lipides, l'effet intergroupe
aurait bien pu être inférieur à la différence
absolue de 4 % que nous avons observée. Enfin, il est important de
noter que les femmes recrutées dans l'étude WINS
différaient de celles de l'étude WHEL en termes de pronostic
après le diagnostic initial, d'âge et de schéma
thérapeutique.
Bien que le régime d'intervention de l'étude WHEL se soit
principalement axé sur l'augmentation de la consommation de
légumes, de fruits et de fibres, il y avait une différence
intergroupe significative dans l'apport de graisse. Cependant, cette
différence peut ne pas avoir été suffisante pour tester
correctement l'hypothèse des graisses alimentaires. À la
différence des changements observés dans les consommations de
légumes, de fruits et de fibres, le changement le plus modeste dans
l'apport en graisses alimentaires était observé chez les
participants du quartile le plus éloigné de l'objectif de
l'étude à l'inclusion. Néanmoins, notre analyse ne
suggérait pas d'effet entre les quartiles initiaux d'apport en lipides,
pas plus que nos résultats n'ont indiqué d'effet de
l'intervention dans les sous-groupes définis par le statut des
récepteurs hormonaux, comme cela a été observé
dans l'étude WINS.
L'absence d'effet sur la survenue de cancer du sein ou sur la
mortalité toutes causes confondues, observée sur la
période de suivi de 7,3 ans de cette étude, n'exclut pas la
possibilité d'une amélioration de la survie à moyen terme
dans cette cohorte. Nous n'avons pas exploré le bénéfice
potentiellement produit par l'augmentation de l'exercice et la perte
pondérale chez les patientes survivant d'un cancer du sein. Enfin,
notre étude n'a pas évalué si l'adoption tôt dans
la vie du régime riche en légumes, en fruits et en fibres et
pauvre en graisses de notre intervention, modifierait le risque de cancer du
sein primaire.
En conclusion, pendant un suivi moyen de 7,3 ans, nous n'avons
trouvé aucune donnée démontrant que l'adoption d'un
régime alimentaire très riche en légumes, en fruits et en
fibres et pauvre en graisses vs un régime de 5 fruits et légumes
par jour, pouvait prévenir la récidive du cancer du sein ou le
décès chez les femmes avec un cancer du sein
précédemment traité au stade précoce.
Informations sur les auteurs
Correspondance: John P. Pierce, PhD, Cancer Prevention and Control
Program, Moores UCSD Cancer Center, University of California, San Diego, La
Jolla, CA 92093-0901
(jppierce{at}ucsd.edu).
Les affiliations des auteurs sont indiquées à la fin
de cet article.
Contributions des auteurs: Le Dr Pierce a eu un accès complet
à toutes les données de l'étude et accepte la
responsabilité de l'exactitude des de l'analyse des données.
Conception et schéma de l'étude: Pierce, Natarajan,
Parker, Greenberg, Carlson, Faerber, Hajek, Jones, Ritenbaugh, Wasserman.
Recueil des données: Caan, Parker, Kealey, Carlson, Gold,
Hollenbach, Karanja, Marshall, Newman, Ritenbaugh, Thomson, Stefanick.
Analyse et interprétation des données: Pierce,
Natarajan, Greenberg, Flatt, Rock, Al-Delaimy, Bardwell, Emond, Faerber, Gold,
Madlensky, Stefanick.
Rédaction du manuscrit: Pierce, Natarajan, Greenberg, Flatt.
Revue critique du manuscrit: Pierce, Natarajan, Caan, Parker,
Greenberg, Flatt, Rock, Kealey, Al-Delaimy, Bardwell, Carlson, Emond, Faerber,
Gold, Hajek, Hollenbach, Jones, Karanja, Madlensky, Marshall, Newman,
Ritenbaugh, Thomson, Wasserman, Stefanick.
Analyse statistique: Natarajan, Flatt, Emond, Marshall.
Obtention du financement: Pierce, Caan, Greenberg, Bardwell, Gold,
Hollenbach, Jones, Marshall, Newman, Ritenbaugh, Wasserman, Stefanick.
Aide administrative, technique ou matérielle: Flatt, Rock,
Kealey, Al-Delaimy, Carlson, Faerber, Hajek, Karanja, Madlensky, Newman.
Supervision de l'étude: Pierce, Natarajan, Caan, Parker, Gold,
Hollenbach, Jones, Karanja, Newman, Thomson, Stefanick.
Liens financiers: Aucun rapporté.
Investigateurs de l'étude WHEL: Equipe de recherché
par centre clinique: WHEL Study Coordinating Center: University of California,
San Diego (UCSD), Cancer Prevention and Control Program, Moores UCSD Cancer
Center, San Diego (John P. Pierce, PhD, Susan Faerber, BA, Barbara A. Parker,
MD, Loki Natarajan, PhD, Cheryl L. Rock, PhD, RD, Vicky A. Newman, MS, RD,
Shirley W. Flatt, MS, Sheila Kealey, MPH, Linda Wasserman, MD, PhD, Wayne A.
Bardwell, PhD, Lisa Madlensky, PhD); Conseillers diététiques de
l'étude WHEL: Sheila K. Fisher, Joyce Bertaux, Leslie Barbier, Sharon
Bonner, Prudy Galagan, Carrie Gonzales, Kaylene Grove, Pam Herskovitz, Susie
Newmiller, Lita Simmons, Susan Wancewicz; Evaluateurs
diététiques de l'étude WHEL: Andrea Jackson, Lita
Simmons, Denice Murillo, Sophie Levy, Nichole Brumley; Analyses biologiques:
Dennis Heath, MS,Mila Pruitt; Centres d'étude: Center for Health
Research-Portland, Portland, Oregon (Njeri Karanja, PhD, Mark U. Rarick, MD,
Lucy Fulton, DTR, RD); Kaiser Permanente Northern California, Oakland (Bette
J. Caan, DrPH, Lou Fehrenbacher, MD, Sarah Josef, RD); Stanford Prevention
Research Center, Stanford University, Stanford, California (Marcia L.
Stefanick, PhD, Robert Carlson, MD, Charlene Kranz, RD, Gwen D'Antoni, RD,
Natalie Ledesma, MS, RD, Monique Schloetter, MS, RD); University of Arizona,
Tucson and Phoenix (Cynthia Thomson, PhD, RD, James Warneke, MD, Cheryl
Ritenbaugh, PhD, MPH, Tina Green, MS, RD, Emily Nardi, MPH, RD); University of
California, Davis (Ellen B. Gold, PhD, Sidney Scudder, MD, Stephanie Burns,
Linda Bresnick); University of California, San Diego, Moores UCSD Cancer
Center, San Diego (Kathryn A. Hollenbach, PhD, Vicky Jones, MD, Michelle
McKinney, Diana Wiggins, RD); University of Texas M. D. Anderson Cancer
Center, Houston (Lovell A. Jones, PhD, Richard Hajek, PhD, Richard Theriault,
DO, Taylor Tran, RD, LD).
Financement/Soutien: L'étude WHEL a été
initiée avec l'aide de la Walton Family Foundation et continuée
grâce au financement d'une bourse de recherche du National Cancer
Institute CA 69375. Certaines données ont été recueillies
dans des centres de recherche clinique généraux (National
Institutes of Health grants M01-RR00070, M01-RR00079, et M01-RR00827).
Rôle du sponsor: Les sponsors qui ont finance n'ont
joué aucun rôle dans le schéma, le développement du
protocole ou la conduite de l'essai ou dans le recueil des données,
l'analyse des données ou la préparation du manuscrit.
Autres Contributions: Nous remercions le comité de
surveillance des données et de la tolérance de l'étude
WHEL (Brian Henderson, MD, Ross Prentice, PhD, Marion Nestle, MPH, PhD, et
Charles Loprinzi, MD) et Sharon Ross, PhD (National Cancer Institute project
officer) pour leur aide à la revue de cet article. Nous remercions
également Kaylene Grove, BS, BA, Christine Hayes, MA, et Hollie Ward,
BA, Cancer Prevention and Control Program, UCSD, pour leur aide administrative
et à la préparation du manuscrit. Enfin, vous sommes
reconnaissants à notre équipe de conseillers
diététiques et aux participants de l'étude WHEL pour leur
dévouement continu à cet essai à long terme.
Affiliations des auteurs: Moores UCSD Cancer Center, University of
California, San Diego, La Jolla; Kaiser Permanente Northern California,
Division of Research, Oakland; Fred Hutchinson Cancer Research Center,
Seattle, Washington; Stanford Comprehensive Cancer Center et Stanford
Prevention Research Center, Stanford University, Stanford, California;
Department of Family and Preventive Medicine, Division of Biostatistics,
University of California, San Diego; Department of Public Health Sciences,
University of California, Davis;M. D. Anderson Cancer Center, University of
Texas, Houston; Center for Health Research, Portland, Oregon; Roswell Park
Cancer Institute, Buffalo, NY; et Department of Family and Community Medicine
et Arizona Cancer Center, Department of Nutritional Sciences, University of
Arizona, Tucson.
BIBLIOGRAPHIE
 |  |
1. Steinmetz KA, Potter JD. Vegetables, fruit, and cancer, II:
mechanisms. Cancer Causes Control.1991; 2(6):427
-442.
PUBMED
2. World Cancer Research Fund. Food, Nutrition and the
Prevention of Cancer: A Global Perspective. Washington, DC: World
Cancer Research Fund, American Institute for Cancer Research;1997
.3. Ingram D. Diet and subsequent survival in women with breast cancer.
Br J Cancer.1994; 69(3):592
-595.
PUBMED
4. Jain M, Miller AB, To T. Premorbid diet and the prognosis of women
with breast cancer. J Natl Cancer Inst.1994; 86(18):1390
-1397.
FREE FULL TEXT
5. Holm LE, Nordevang E, Hjalmar ML, Lidbrink E, Callmer E, Nilsson B.
Treatment failure and dietary habits in women with breast cancer. J
Natl Cancer Inst.1993; 85(1):32
-36.
FREE FULL TEXT
6. Rohan TE, Hiller JE, McMichael AJ. Dietary factors and survival
from breast cancer. Nutr Cancer.1993; 20(2):167
-177.
PUBMED
7. Zhang S, Folsom AR, Sellers TA, Kushi LH, Potter JD. Better breast
cancer survival for postmenopausal women who are less overweight and eat less
fat: the Iowa Women's Health Study. Cancer.1995; 76(2):275
-283.
PUBMED
8. Nomura AM, Marchand LL, Kolonel LN, Hankin JH. The effect of
dietary fat on breast cancer survival among Caucasian and Japanese women in
Hawaii. Breast Cancer Res Treat.1991; 18(suppl 1):S135
-S141.
PUBMED
9. Gregorio DI, Emrich LJ, Graham S, Marshall JR, Nemoto T. Dietary
fat consumption and survival among women with breast cancer. J Natl
Cancer Inst.1985; 75(1):37
-41.
PUBMED
10. Rock CL, Demark-Wahnefried W. Nutrition and survival after the
diagnosis of breast cancer: a review of the evidence. J Clin
Oncol.2002; 20(15):3302
-3316.
FREE FULL TEXT
11. Mai V, Kant AK, Flood A, Lacey JV Jr, Schairer C, Schatzkin A. Diet
quality and subsequent cancer incidence and mortality in a prospective cohort
of women. Int J Epidemiol.2005; 34(1):54
-60.
FREE FULL TEXT
12. Kroenke CH, Fung TT, Hu FB, Holmes MD. Dietary patterns and
survival after breast cancer diagnosis. J Clin Oncol.2005; 23(36):9295
-9303.
FREE FULL TEXT
13. Rock CL, Flatt SW, Natarajan L, et al. Plasma carotenoids and
recurrence-free survival in women with a history of breast cancer.
J Clin Oncol.2005; 23(27):6631
-6638.
FREE FULL TEXT
14. Pierce JP, Stefanick ML, Flatt SW, et al. Greater survival after
breast cancer in physically active women with high vegetable-fruit intake
regardless of obesity. J Clin Oncol.2007; 25(17):2345
-2351.
FREE FULL TEXT
15. McEligot AJ, Largent J, Ziogas A, Peel D, Anton-Culver H. Dietary
fat, fiber, vegetable, and micronutrients are associated with overall survival
in postmenopausal women diagnosed with breast cancer. Nutr
Cancer.2006; 55(2):132
-140.
PUBMED
16. Davies AA, Davey Smith G, Harbord R, et al. Nutritional
interventions and outcome in patients with cancer or preinvasive lesions:
systematic review. J Natl Cancer Inst.2006; 98(14):961
-973.
FREE FULL TEXT
17. Harashima E, Nakagawa Y, Urata G, Tsuji K, Shirataka M, Matsumura
Y. Time-lag estimate between dietary intake and breast cancer mortality in
Japan. Asia Pac J Clin Nutr.2007; 16(1):193
-198.
PUBMED
18. Chlebowski RT, Blackburn GL, Thomson CA, et al. Dietary fat
reduction and breast cancer outcome: interim efficacy results from the Women's
Intervention Nutrition Study. J Natl Cancer Inst.2006; 98(24):1767
-1776.
FREE FULL TEXT
19. Clark C. Study will put folklore on diet to test. San
Diego Union-Tribune. March 11,1998
: A1, A17.20. Pierce JP, Faerber S, Wright FA, et al. A randomized trial of the
effect of a plant-based dietary pattern on additional breast cancer events and
survival: the Women's Healthy Eating and Living (WHEL) Study.
Control Clin Trials.2002; 23(6):728
-756.
PUBMED
21. Pierce JP, Newman VA, Flatt SW, et al. Telephone counseling
intervention increases intakes of micronutrient- and phytochemical-rich
vegetables, fruit and fiber in breast cancer survivors. J
Nutr.2004; 134(2):452
-458.
FREE FULL TEXT
22. National Cancer Institute. Action Guide for Healthy
Eating. Bethesda, MD: National Cancer Institute;1995
.23. National Cancer Institute. Eat 5 Fruits and Vegetables a
Day. Washington, DC: National Cancer Institute;1995
.24. Lachin JM, Foulkes MA. Evaluation of sample size and power for
analyses of survival with allowance for nonuniform patient entry, losses to
follow-up, non-compliance, and stratification.
Biometrics.1986; 42(3):507
-519.
PUBMED
25. Bandura A. Social Foundations of Thought and Action: A
Social Cognitive Theory. Englewood Cliffs, NJ: Prentice Hall;1986
.26. US Department of Agriculture/US Department of Health and Human
Services. Dietary Guidelines for Americans: Home Health and Garden
Bulletin No. 232. Washington, DC: US Dept of Health and Human
Services; 1995.27. Little RJA, Rubin DB. Statistical Analysis With Missing
Data. New York, NY: John Wiley & Sons;1987
.28. Myriad Genetic Laboratories. BRCA risk calculator and
mutation prevalence tables.
http://www.myriadtests.com/provider/brca-mutation-prevalence.htm.
Accessed June 4, 2007.29. Women's Health Initiative. WHI Personal Habits Questionnaire.
http://www.whiscience.org/data/forms/F34v2.pdf.
Accessed June 4, 2007.30. Johnson-Kozlow M, Rock CL, Gilpin EA, Hollenbach KA, Pierce JP.
Validation of the WHI Brief Physical Activity Questionnaire among women
diagnosed with breast cancer. Am J Health Behav.2007; 31(2):193
-202.
PUBMED
31. Hong S, Bardwell WA, Natarajan L, et al. Correlates of physical
activity level in breast cancer survivors participating in the Women's Healthy
Eating and Living (WHEL) Study. Breast Cancer Res
Treat.2007; 101(2):225
-232.
PUBMED
32. Women's Health Initiative. WHI Thoughts and Feelings Questionnaire.
http://www.whiscience.org/data/dd_byset/f37_dd.pdf.
Accessed June 4, 2007.33. Therneau TM, Grambsch PM. Modeling Survival Data:
Extending the Cox Model, Statistics for Biology and Health. New
York, NY: Springer-Verlag; 2000.34. Rock CL, Flatt SW, Thomson CA, et al. Plasma triacylglycerol and
HDL cholesterol concentrations confirm self-reported changes in carbohydrate
and fat intakes in women in a diet intervention trial. J
Nutr.2004; 134(2):342
-347.
FREE FULL TEXT
35. Jatoi I, Chen BE, Anderson WF, Rosenberg PS. Breast cancer
mortality trends in the United States according to estrogen receptor status
and age at diagnosis. J Clin Oncol.2007; 25(13):1683
-1690.
FREE FULL TEXT
36. Bardwell W, Major J, Pierce JP. Quality of life change in breast
cancer survivors participating in the Women's Healthy Eating and Living (WHEL)
Study. Ann Behav Med.2003; 25(suppl):52
.
37. Thomson CA, Flatt SW, Rock CL, Ritenbaugh C, Newman V, Pierce JP.
Increased fruit, vegetable and fiber intake and lower fat intake reported
among women previously treated for invasive breast cancer. J Am
Diet Assoc.2002; 102(6):801
-808.
PUBMED
38. Caan B, Sternfeld B, Gunderson E, Coates A, Quesenberry C, Slattery
ML. Life After Cancer Epidemiology (LACE) study: a cohort of early stage
breast cancer survivors (United States). Cancer Causes
Control.2005; 16(5):545
-556.
PUBMED
39. Wayne SJ, Lopez ST, Butler LM, Baumgartner KB, Baumgartner RN,
Ballard-Barbash R. Changes in dietary intake after diagnosis of breast cancer.
J Am Diet Assoc.2004; 104(10):1561
-1568.
PUBMED
40. Pierce JP, Natarajan L, Marshall J, Messer K. Dietary fat reduction
and breast cancer outcome: interim efficacy results from the Women's
Intervention Nutrition Study [letter]. J Natl Cancer
Inst. 2007;99
(11):900
.
FREE FULL TEXT
41. Thiébaut AC, Schatzkin A, Ballard-Barbash R, Kipnis V.
Dietary fat and breast cancer: contributions from a survival trial.
J Natl Cancer Inst.2006; 98(24):1753
-1755.
FREE FULL TEXT
ARTICLES EN RAPPORT
Cette semaine dans le JAMA
JAMA. 2007;298:257.
Texte Complet
Matières grasses, fruits, légumes et chances de survie après un cancer du sein
Susan M. Gapstur et Seema Khan
JAMA. 2007;298:335-336.
Texte Complet
|