 |
 |

Immunogénicité d'un vaccin glycoconjugué tétravalent anti-méningococcique chez les nourrissonsUn essai randomisé et comparatif
Matthew D. Snape, FRACP;
Kirsten P. Perrett, MBBS;
Karen J. Ford, BN;
Tessa M. John, MA;
David Pace, MRCPLH;
Ly-Mee Yu, MSc;
Joanne M. Langley, MD;
Shelley McNeil, MD;
Peter M. Dull, MD;
Francesca Ceddia, MD;
Alessandra Anemona, DStat;
Scott A. Halperin, MD;
Simon Dobson, MD;
Andrew J. Pollard, PhD
RÉSUMÉ
 |  |
Contexte L'immunisation par un vaccin glycoconjugué
quadrivalent méningococcique (sérogroupe ACWY) est
recommandée chez tous les adolescents des USA. Cependant, le vaccin
actuellement autorisé est médiocrement immunogène dans la
petite enfance, où sont observés les taux les plus
élevés de cette maladie.
Objectif Déterminer l'immunogénicité d'un
vaccin méningococcique quadrivalent original CRM197-conjugué
(MenACWY) chez des enfants en bas âge.
Schéma, environnement et participants Étude
randomisée, en ouvert, contrôlée chez 225 nourrissons
âgés de 2 mois au Royaume-Uni et 196 au Canada d'août 2004
à septembre 2006.
Traitement Les enfants en bas âge au Royaume Uni ont
reçu un protocole primaire de MenACWY (à 2, 3, et 4 mois ou
à 2 et 4 mois) ou un vaccin de Neisseria meningitidis
glycoconjugué méningococcique monovalent du sérogroupe C
(MenC) (à 2 et à 4 mois). Tous ont reçu MenACWY à
12 mois. Les nourrissons canadiens ont reçu MenACWY à 2, 4, et 6
mois ou à 2 et 4 mois; à 12 mois ils ont reçu MenACWY, un
vaccin quadrivalent simple polysaccharidique, ou aucun vaccin.
Résultats Selon l'analyse pré-spécifiée
per-protocole, les pourcentages (IC 95%) de répondeurs pour MenACWY
à 2, 3, et 4 mois après l'immunisation primaire avec des titres
hSBA 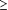 1/4 ont été pour le sérogroupe A, 93% (84%-98%)
; pour le C, 96% (89%-99%) ; pour W-135, 97% (90%-100%) ; et pour Y, 94%
(86%-98%). Avec une analyse en intention-à-traiter post-hoc en imputant
des valeurs pour les données absentes, ces variables sont
restées inchangées pour les sérogroupes C et Y ; pour le
sérogroupe A, les variables étaient de 92% (84%-97%), et pour
W-135, de 97% (91%-99%). Dans l'analyse per-protocole des receveurs de MenACWY
à 2, 4, et 6 mois, les pourcentages (IC 95%) de répondeurs
étaient pour A, 81% (71%-89%) ; C, 98% (92%-100%) ; W-135,99%
(93%-100%) ; et Y, 98% (92%-100%). Avec l'analyse des valeurs imputées,
ces valeurs étaient pour A, 83% (74%-89%) ; C, 98% (93%-99%) ; W-135,
99% (94%-100%) ; et Y, 98% (92%-99%). Au moins 84% des receveurs de MenACWY 2
et 4 mois ont atteint un titre hSBA 1/4 ont été pour le sérogroupe A, 93% (84%-98%)
; pour le C, 96% (89%-99%) ; pour W-135, 97% (90%-100%) ; et pour Y, 94%
(86%-98%). Avec une analyse en intention-à-traiter post-hoc en imputant
des valeurs pour les données absentes, ces variables sont
restées inchangées pour les sérogroupes C et Y ; pour le
sérogroupe A, les variables étaient de 92% (84%-97%), et pour
W-135, de 97% (91%-99%). Dans l'analyse per-protocole des receveurs de MenACWY
à 2, 4, et 6 mois, les pourcentages (IC 95%) de répondeurs
étaient pour A, 81% (71%-89%) ; C, 98% (92%-100%) ; W-135,99%
(93%-100%) ; et Y, 98% (92%-100%). Avec l'analyse des valeurs imputées,
ces valeurs étaient pour A, 83% (74%-89%) ; C, 98% (93%-99%) ; W-135,
99% (94%-100%) ; et Y, 98% (92%-99%). Au moins 84% des receveurs de MenACWY 2
et 4 mois ont atteint un titre hSBA 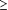 1/4 pour les sérogroupes C,
W-135, et Y après l'immunisation primaire, de même qu'ont fait au
moins 60% des receveurs pour le sérogroupe A (analyse per-protocole et
d'imputation). Au moins 95% des receveurs primaires et du rappel de MenACWY
ont atteint des titres de hSBA 1/4 pour les sérogroupes C,
W-135, et Y après l'immunisation primaire, de même qu'ont fait au
moins 60% des receveurs pour le sérogroupe A (analyse per-protocole et
d'imputation). Au moins 95% des receveurs primaires et du rappel de MenACWY
ont atteint des titres de hSBA 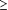 1/4 pour les sérogroupes C, W-135,
et Y à 13 mois, de même qu'au moins 84% pour le sérogroupe
A (analyse per-protocole et analyse d'imputation). Au cours du protocole
d'immunisation primaire, une douleur après immunisation lors des
mouvements de la jambe a été observée chez 2% des
receveurs de UKMenACWY 2 et 4 mois et chez 4% de MenC 2 et 4 mois ; une
température de 38°C ou plus a été observée
respectivement chez 4% et 2% des receveurs de ces groupes. 1/4 pour les sérogroupes C, W-135,
et Y à 13 mois, de même qu'au moins 84% pour le sérogroupe
A (analyse per-protocole et analyse d'imputation). Au cours du protocole
d'immunisation primaire, une douleur après immunisation lors des
mouvements de la jambe a été observée chez 2% des
receveurs de UKMenACWY 2 et 4 mois et chez 4% de MenC 2 et 4 mois ; une
température de 38°C ou plus a été observée
respectivement chez 4% et 2% des receveurs de ces groupes.
Conclusion MenACWY est bien toléré et
immunogène chez les nourrissons.
Trial Registration
clinicaltrials.gov
Identifier: NCT00262002
JAMA.
2008;299(1):39-52
Affiliations des auteurs: Oxford Vaccine Group, University of
Oxford, England; Centre for Statistics in Medicine, Oxford, England; Canadian
Center for Vaccinology, Dalhousie University, Halifax, Nova Scotia, Canada;
IWK Health Center, Halifax; Queen Elizabeth II Health Sciences Center,
Halifax; Novartis Vaccines and Diagnostics, Siena, Italy; Vaccine Evaluation
Center, British Columbia Children's Hospital, Vancouver, British Columbia,
Canada.
ARTICLES EN RAPPORT
Un vaccin multivalent conjugé dans la prévention de la maladie méningococcique chez les nourrissons
Lee H. Harrison
JAMA. 2008;299:217-220.
Texte Complet
Cette semaine dans le JAMA
JAMA. 2008;299:9.
Texte Complet
|